K.A. Castillo–Rosales, C. D. Arrieta–González*, E. García–Hernández, Z. Vargas–Galarza
Tecnológico Nacional de México, Instituto Tecnológico de Zacatepec, Calzada Instituto Tecnológico 27, 62780 Zacatepec, Morelos, México. Correo electrónico: cdaglez@gmail.com
Recibido: Febrero de 2020; Aceptado: Abril de 2020
Texto completo (pdf)
Cita (APA)
Castillo–Rosales, K.A., Arrieta–González, C. D., García–Hernández, E., Vargas–Galarza, Z. (2020). Efecto del aloe vera en la capacidad antimicrobiana de películas quitosano/pva/nanoarcilla. Revista Iberoamericana de Polímeros, 21(3), 96-106.
RESUMEN
Se obtuvieron películas poliméricas quitosano/PVA/nanoarcilla con diferentes concentraciones de cada constituyente. Se realizó la caracterización fisicoquímica y mecánica de las películas poliméricas mediante ensayos de FTIR, solubilidad, calorimetría diferencial de barrido, medición de espesores y ensayos mecánicos. Los resultados mostraron que tanto la concentración de quitosano como la concentración de nanoarcilla afecta tanto las propiedades fisicoquímicas como mecánicas de las películas poliméricas. De manera similar, la capacidad de absorción de Aloe Vera está influenciada por la concentración quitosano y nanoarcilla. La capacidad antimicrobiana de las películas fue evaluada con Staphylococcus aureus y Escherichia coli. Todas las películas mostraron una buena capacidad antimicrobiana en presencia de Staphylococcus aureus y la adición de Aloe Vera la incrementó, sin embargo, en presencia de Escherichia coli no fue observada capacidad antimicrobiana en ninguno de los casos evaluados.
ABSTRACT
Polymeric chitosan/PVA/nano–clay films with different concentrations of each constituent were obtained. Physicochemical and mechanical characterization of the polymeric films was performed. FT–IR, solubility, differential scanning calorimetry, thickness measurement and mechanical tests were performed. The results showed that the concentration of chitosan and nano–clay affects both the physicochemical and mechanical properties of the polymeric films. Similarly, the absorption capacity of Aloe Vera is influenced by the chitosan and nano–clay concentration. The antimicrobial capacity of the films was evaluated with Staphylococcus aureus and Escherichia coli. All films showed a good antimicrobial capacity in the presence of Staphylococcus aureus and the addition of Aloe Vera increased it, however, in the presence of Escherichia coli no antimicrobial capacity was observed in any of the cases evaluated.
INTRODUCCIÓN
Los avances tecnológicos a lo largo de la historia han estado íntimamente ligados a la investigación y/o desarrollo de nuevos materiales que presenten mejores propiedades mecánicas, de barrera, aislamiento y térmicas. El uso de materiales compuestos se emplean desde la antigüedad, los primeros biomateriales poliméricos utilizados fueron la celulosa y la seda, los cuales se emplearon como apósitos para heridas y suturas, respectivamente, sin embargo, nuevas tecnologías emplean materiales compuestos para diversas aplicaciones, algunas enfocándose en el área biomédica en especialmente de ingeniería de tejidos y medicina regenerativa. Los materiales usados en estas disciplinas deben ser biocompatibles y proporcionar un ambiente mecánico donde el nuevo tejido pueda ser sometido al estrés normal de la célula, ser porosos y permeables para permitir el ingreso de nutrientes a las células y disponer de una estructura superficial adecuada para que las células se adhieran [1].
Por otra parte, la utilización de fibras sintéticas elaboradas con poliéster y nylon para el uso de vendajes y apósitos, dañan al medio ambiente, además utilizan un altoconsumo energético y en su proceso diversas sustancias químicas que perjudican a la salud [2]. El desarrollo de biomateriales compuestos para aplicaciones médicas e industriales están optando por elaborar materiales compuestos con fuentes renovables que no dañen al medio ambiente mediante el uso de biopolímeros y extractos naturales, gracias a sus propiedades funcionales es actualmente una de las opciones más prometedoras para el desarrollo de materiales [3].
En la literatura se reporta el uso de polímeros naturales a base de proteínas, poliésteres y polisacáridos, utilizando quitosano debido a su biocompatibilidad y por sus propiedades antimicrobianas, mecánicas y de barrera. De igual forma, se cita la elaboración de apósitos a base de extractos naturales usando Aloe vera, por sus amplias aplicaciones medicinales y curativas, adicionando nanopartículas como nanoantibióticos contra aislados bacterianos clínicos resistentes a múltiples fármacos.
Dado a lo anterior, en este trabajo se propone elaborar materiales compuestos a base de quitosano/PVA/nanoarcilla como refuerzo y extracto de Aloe Vera, para su posible uso como apósitos o vendajes, utilizando fuentes renovables.
PROCEDIMIENTO EXPERIMENTAL
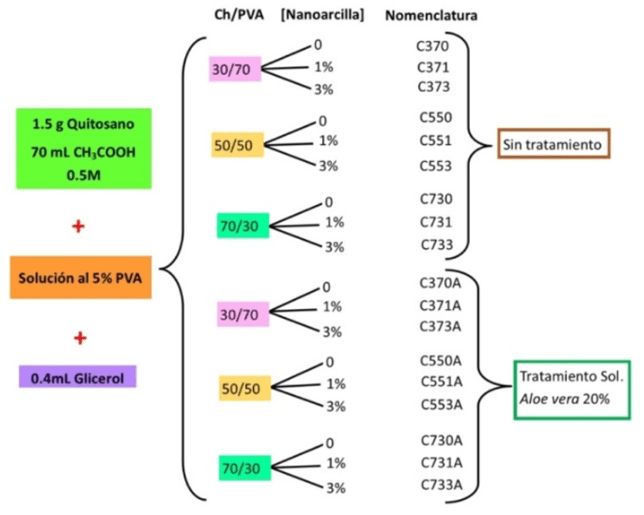
Preparación de las películas. Para la obtención de las películas se disolvió quitosano de bajo peso molecular en una solución de ácido acético 0,5 M hasta su homogenización durante 2 h en agitación magnética, posteriormente se preparó una solución acuosa de 5% de PVA disolviéndolo con agitación constante durante 30 min a 70°C. Para la elaboración del material compuesto, se mantuvo en agitación la solución de quitosano durante 10 min, se adicionaron las cantidades correspondientes de nanoarcilla (0, 1, y 3% w/w respecto al quitosano) manteniéndose en agitación magnética durante 20 min, posteriormente, se añadieron 0,4 mL de glicerol y se mantuvo en agitación, para una mayor dispersión de las nanopartículas. La solución fue sometida a baño ultrasónico durante 90 min, posteriormente se adicionó la solución de PVA para obtener concentraciones 30/70, 50/50, y 70/30 v/v (Quitosano/PVA) manteniéndose en agitación magnética durante 20 min a temperatura ambiente, continuando en el baño ultrasónico con calor durante 20 min. Las mezclas resultantes se vertieron en moldes de vidrio de 11·16 cm a una temperatura de 23°C. Se dejó secar y solidificar por tres días y se procedió a desprender las películas y almacenarlas en bolsas con cierre hermético para su caracterización. La Figura 1 muestra la matriz de trabajo y por simplicidad la nomenclatura asignada a cada formulación.
Caracterización fisicoquímica. Las pruebas de FTIR a las películas obtenidas se realizaron en un espectrofotómetro de FTIR–ATR marca Perkin Elmer Spectrum Two con software Spectrum®, las muestras se analizaron en el modo de transmitancia con un intervalo de 650 a 4.000 cm–1, con una resolución de 4 cm–1 y 16 barridos, utilizando el accesorio de ATR (Reflectancia Total Atenuada).
Se determinó la solubilidad en de las películas de acuerdo a ASTM D 570–98 [4]. Para ello se cortaron dos muestras de cada formulación con dimensiones de 2·2 cm [5]. Éstas se colocaron en viales de plástico de 50 mL, posteriormente se adicionaron 30 mL de agua baja en sales en cada vial y se dejaron en reposo durante 24 horas a 21,4°C. Posteriormente se decantó el agua y los residuos de las películas se colocaron en una celda de aluminio y secaron durante 24 horas a 100°C. Finalmente el porcentaje de solubilidad se calculó de acuerdo a:
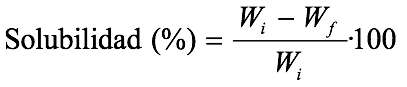
dónde Wi y Wf son los pesos iniciales y finales respectivamente de las películas [6].
Las películas fueron sometidas a análisis de calorimetría diferencial de barrido en un equipo TA Instrument DSC 2100 New Castle. Se tomaron de 7 a 8 mg de muestra colocándose en cápsulas de aluminio, siendo selladas herméticamente utilizando una prensa mecánica, como referencia se utilizó una charola de aluminio vacía. La muestra se sometió a un programa de calentamiento en el intervalo de 25 a 300°C y una velocidad de calentamiento de 10°C/min, generando una atmósfera inerte en la celda por circulación de 50 mL/min de gas nitrógeno (pureza 99,9%). Los resultados fueron analizados con el programa TA Instruments Universal Analysis 2000.
Caracterización mecánica. Una vez obtenidas las diferentes películas se midió su espesor con ayuda de un micrómetro Digimatic IP65 Mitutoyo, modelo MDC–1 MJ, con un error permisible de ± 0,00005, registrando 10 mediciones aleatorias para cada película y verificando que el espesor promedio no fuera mayor a 1 mm [7].
Las propiedades mecánicas de las películas se determinaron de acuerdo a ASTM D882–02 [8]. Se empleó una máquina universal BlueHill Lite de INSTRON Modelo 2519–107. Mediante los ensayos de tensión se determinó el esfuerzo máximo de tensión a la fractura, porcentaje de deformación y módulo de Young. Los ensayos se realizaron por triplicado, previamente las muestras se cortaron en rectángulos de 1·10 cm y se sometieron a una humedad relativa de 50 ± 5% durante 42 horas antes de realizar los ensayos [9].
Caracterización antimicrobiana. La caracterización antimicrobiana de las películas se realizó con y sin la impregnación de Aloe vera. En el caso de las películas con impregnación de Aloe vera, previamente se determinó su capacidad de absorción. Para ello, muestras con dimensiones de 2·2 cm impregnaron en una solución de Aloe vera al 20% durante 8 horas. Se realizaron mediciones del cambio de peso en una balanza electrónica cada dos horas para lograr un peso constante. El porcentaje de absorción se determinó de acuerdo a:
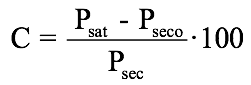
donde C es la capacidad de absorción, Psat el peso saturado y Pseco el peso seco.
La capacidad antimicrobiana se llevó a cabo en presencia de dos especies bacterianas: Staphylococcus aureus y Escherichia coli, evaluando el diámetro del halo de inhibición. El procedimiento consistió en la preparación de agar de soya al 1,5% g/V y se vertieron 80 mL en una cápsula de Petri, una vez gelificado se colocó una capa de 80 mL de agar LB al 0,8% g/V y se inoculó con 1,6 mL de concentración bacteriana usando de referencia 6·108 UFC/mL de acuerdo a los estándares de McFarland. Una vez que la capa de agar con bacterias solidificó, se colocaron cada una de las películas previamente esterilizadas mediante rayos UV. Finalmente, las cajas se mantuvieron a 4°C durante 4 horas para permitir la difusión de los microorganismos en el agar, y posteriormente se incubaron por un periodo de 24 h a 37°C.
RESULTADOS Y DISCUSIÓN
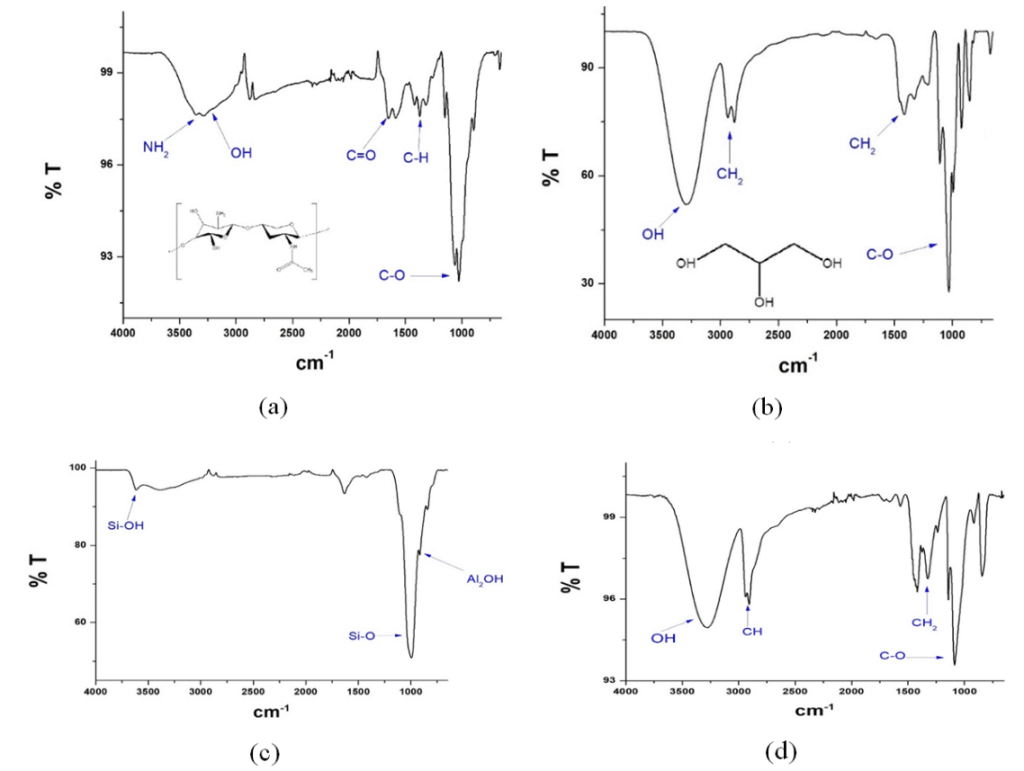
Caracterización fisicoquímica. La Figura 2 muestra los espectros FTIR de los compuestos precursores de las películas fabricadas. Respecto al quitosano, se observan los 2 picos característicos del grupo amino que se encuentra en el intervalo de 3.000 a 3.500 cm–1, así como el grupo OH, en la región de 1.700 a 1.800 cm–1 se encuentra el estiramiento C = O, entre 1400–1500 cm–1 se encuentra la flexión del C–H y entre 1.900 a 1.200 cm–1 se observa el estiramiento C–O. El espectro FTIR del glicerol muestra el estiramiento del grupo O – H en el rango de 3.000 a 3.500 cm–1, y entre 2.900–3.000 cm–1 se encuentra el movimiento asimétrico de CH2 y de 1.400 a 1.500 cm–1 la flexión del CH2, mientras que de 900 a 1.200 cm–1 se encuentra el estiramiento C–O. Del espectro FTIR de la nanoarcilla se observa el estiramiento Si–OH en el intervalo de 3.500–3.700 cm–1, en 1.000 cm–1 se observa el estiramiento Si – O, y en 914 cm–1 se encuentra la vibración correspondiente al Al2OH. Del espectro FTIR del PVA se observan las señales del estiramiento O – H en la región de 3.000–3.500 cm–1, de 2.900–3.000 cm–1 se observa el movimiento asimétrico y simétrico del CH2, de 1.200–1.500 cm–1 se encuentra la flexión de CH2 y de 1.000–1.200 cm–1 se encuentra el estiramiento C – O.
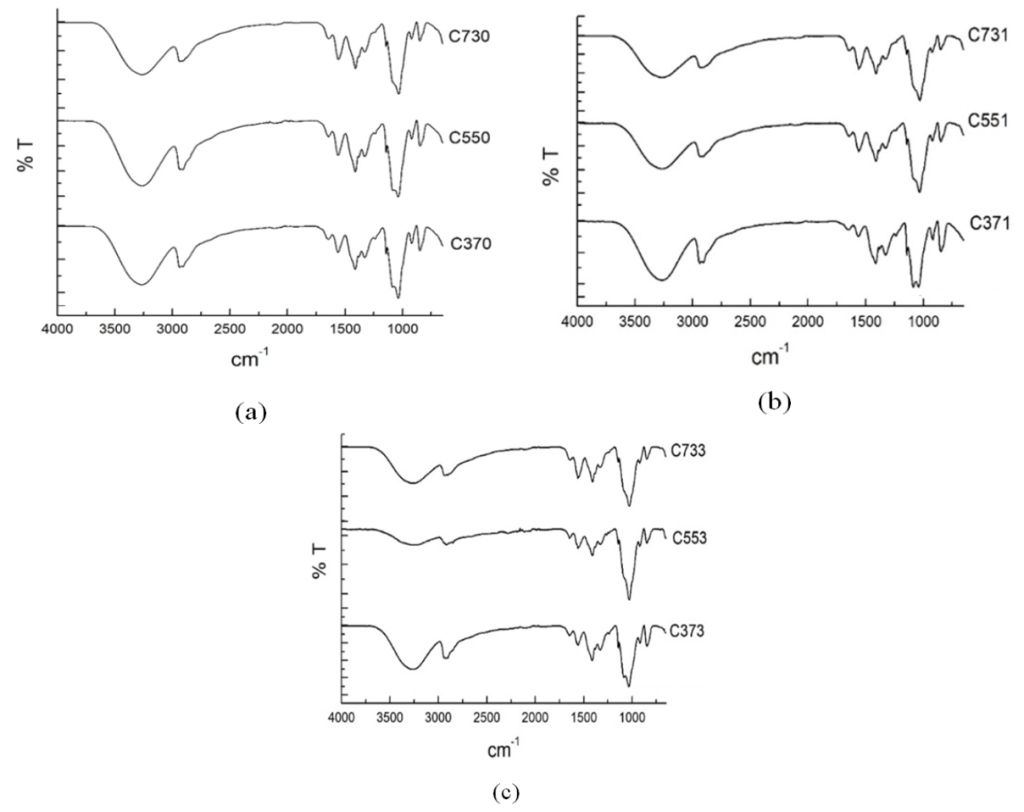
La Figura 3 muestra los espectros FTIR de las diferentes películas evaluadas. En general se observa que los distintos espectros representan una sobreposición de los distintos espectros individuales de cada compuesto (Figura 2). La Figura 3a muestra el efecto de la concentración de PVA, en el intervalo de 3.000–3.500 cm–1 se muestra el estiramiento del grupo hidroxilo, aproximadamente en 1.600 cm–1 se presenta el estiramiento C = O y en 1.100 cm–1 se encuentra el estiramiento C – O, se observa un aumento de la señal del estiramiento O – H, NH2 y del estiramiento C – O a medida que se incrementa la concentración de quitosano y PVA [10]. Con la adición de nanoarcilla (Figuras 3b y 3c) en el intervalo de 3.000 a 3.500 cm–1 se observa el estiramiento OH, aproximadamente en 1.100 cm–1 se observa el estiramiento de C – O, por otra parte, de 1.600–1.700 cm–1 se muestra el estiramiento C = O, además en 914 cm–1 se encuentra la vibración correspondiente a Al2OH de la nanoarcilla y el estiramiento Si – O de 1.000 a 1.200 cm–1.
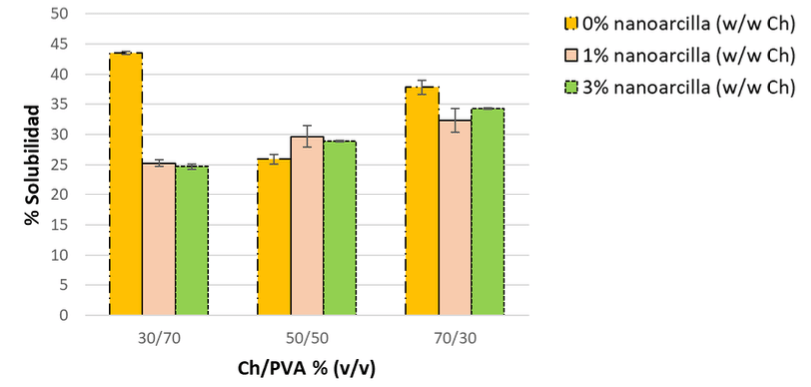
La Figura 4 muestra los resultados de solubilidad de las distintas películas evaluadas. En general se observa que, en ausencia de nanoarcilla, las películas 50/50 (Quitosano/ PVA) muestran la menor solubilidad, y en presencia de nanoarcilla la solubilidad disminuye. En particular, las películas 50/50 (Quitosano/PVA) con y sin adición de nanoarcilla, son las que menos variación mostraron en su solubilidad con un valor promedio entre 25–30%.
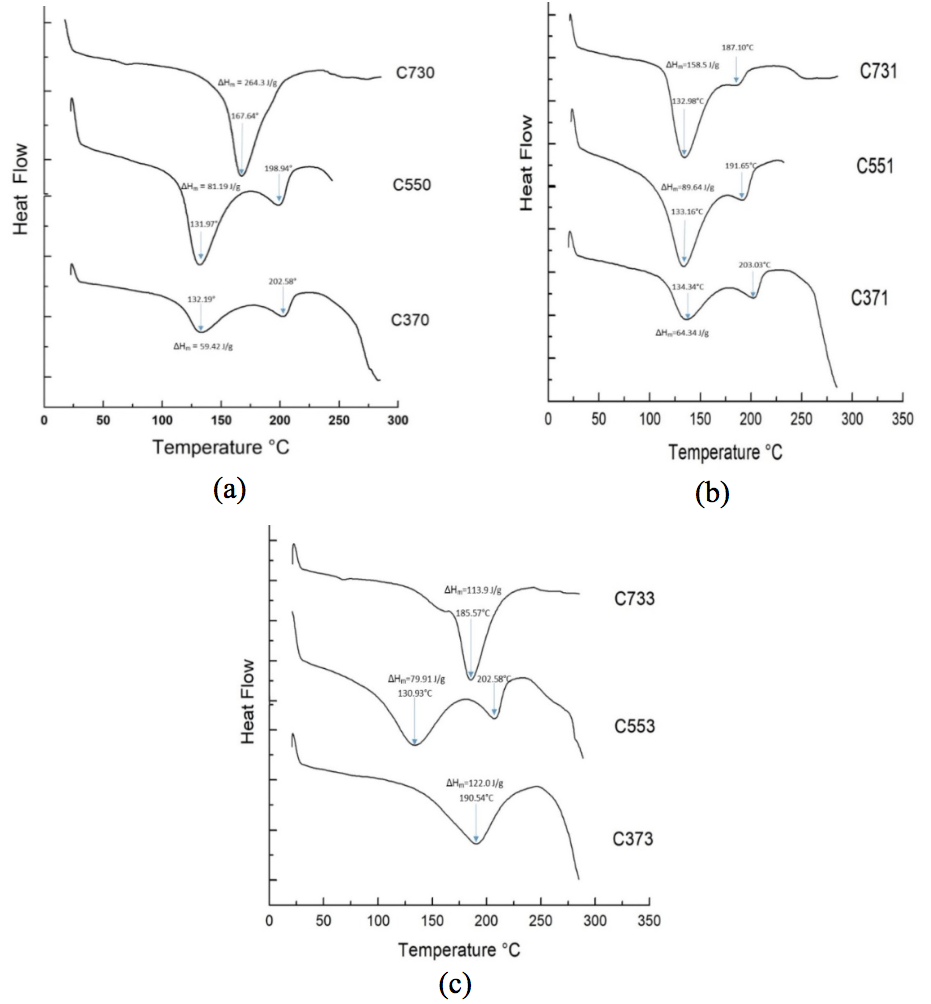
La Figura 5 muestra los espectros DSC de las películas evaluadas. En ausencia de nanoarcilla (Figura 5a) las muestras C370 y C550 exhiben dos picos entre 131 y 203°C, y al incrementar la concentración de quitosano (muestra C730) se observa solo la presencia de un pico en 167,64°C, esto puede ser debido a una mayor homogenización de las películas debido a la mayor concentración de quitosano. Con la adición de 1% de nanoarcilla (Figura 5b), todas las películas presentan dos picos indicando una temperatura de fusión en un intervalo de 133 a 204°C, siendo la película con menor contenido de quitosano (muestra C371) la que mayor punto de fusión presentó (134,34–203,03°C). Con la adición de 3% de nanoarcilla se observó que las muestras C733 y C373 presentan un solo pico en el intervalo de 185 a 191°C.
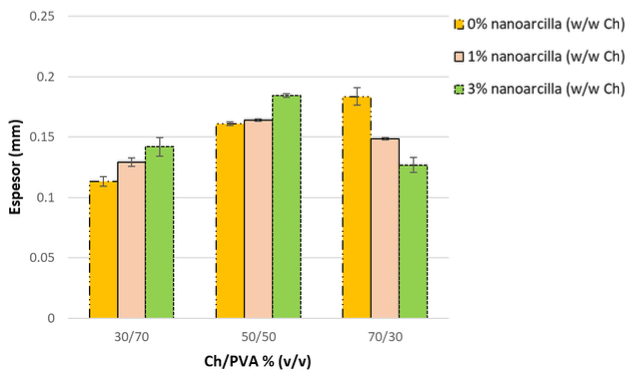
Caracterización física y mecánica. La Figura 6 muestra el efecto de la concentración de PVA y nanoarcilla sobre el espesor de las películas obtenidas. Se observa que en ausencia de nanoarcilla, el espesor de las películas incrementa al aumentar la concentración de quitosano. Por otro lado, en presencia de nanoarcilla, los mayores espesores fueron obtenidos con las formulaciones 50/50 (Quitosano/PVA).
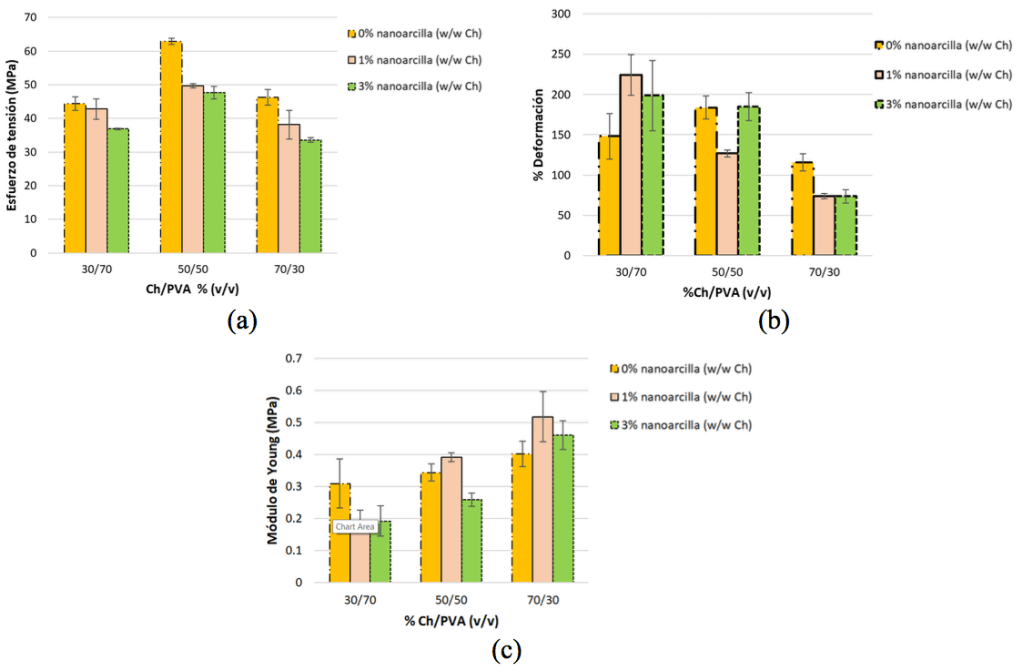
La Figura 7 muestra los resultados de las pruebas mecánicas realizadas a las diferentes películas. En cuanto al esfuerzo a la tensión, se observa que en ausencia de nanoarcilla las formulación 50/50 (Quitosano/PVA) exhibe el mayor valor, y en general, la adición de nanoarcilla tiende a disminuir esta propiedad. Respecto al porcentaje de deformación, de nueva cuenta se observa que en ausencia de nanoarcilla, la formulación 50/50 (Quitosano/PVA) muestra el mayor porcentaje de deformación, sin embargo, en presencia de nanoarcilla el porcentaje de deformación incrementa al aumentar la concentración de PVA. Por otro lado, respecto al módulo de Young, se observa que en ausencia de nanoarcilla, el módulo de Young de las películas incrementa al aumentar el contenido de quitosano, y en presencia de nanoarcilla sólo las películas con mayor concentración de quitosano muestran un incremento con la adición de nanoarcilla a las dos concentraciones evaluadas. En general se observó que debido a la incorporación de nanoarcilla, las propiedades mecánicas de las películas obtenidas fueron mayores (resistencia y flexibilidad) [11, 12].
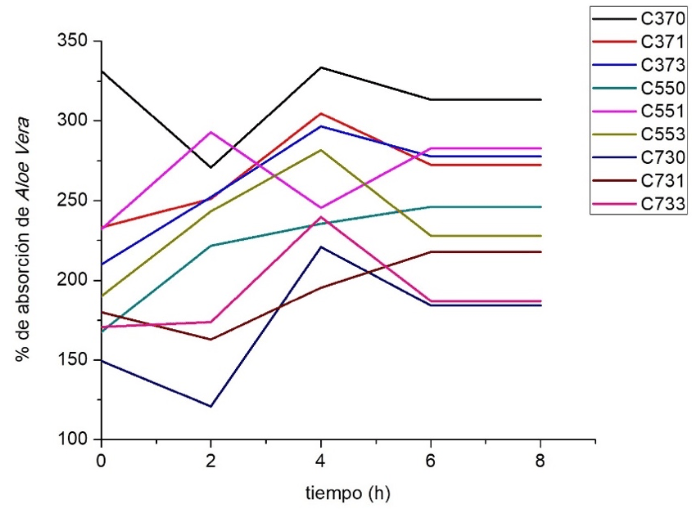
Caracterización antimicrobiana. La actividad antimicrobiana de las películas se realizó para las especies de Staphylococcus aureus (S. aureus) y Escherichia coli (E.coli) midiendo el diámetro del halo de inhibición. Las películas fueron evaluadas con y sin la absorción de Aloe vera. La Figura 8 muestra los resultados de los ensayos de absorción de Aloe vera. Los resultados muestran que todas las películas mostraron una absorción mayor al 100% de su peso, la película que presentó el mayor porcentaje (> 300%) de absorción fue la C370. En general, al incrementar la concentración de quitosano el porcentaje de absorción tiende a disminuir.
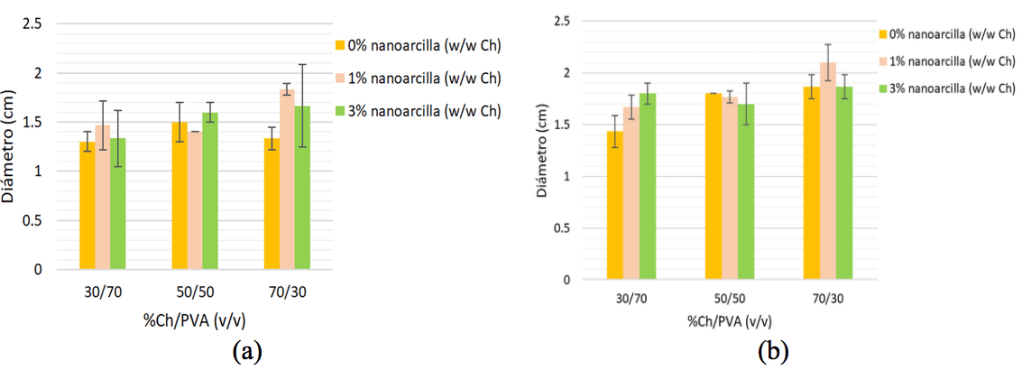
Los resultados obtenidos mostraron que las películas no presentaron halo de inhibición en el caso de E. Coli, sin embargo, en presencia de S. aureus si se observó un halo de inhibición. En la Figura 9a se presenta el diámetro del halo de inhibición obtenido por las muestras sin Aloe vera, observando que las muestras con mayor diámetro de halo de inhibición son las que presentan mayor concentración de quitosano y nanoarcilla. La Figura 9b muestra el diámetro del halo de inhibición de las películas después de su inmersión en la solución de Aloe vera. En general se observó que el halo de inhibición fue mayor, y que éste sigue la misma tendencia que la observada en ausencia de Aloe vera, es decir, incrementa con la concentración de quitosano y nanoarcilla.
CONCLUSIONES
De acuerdo a las pruebas realizadas, las muestras podrían ser factibles para ser un hidrogel y usarlo como apósito, debido a que presentan una solubilidad menor de 45%, mayor resistencia y mayor porcentaje de deformación. Los análisis FTIR, muestran interacciones en los grupos funcionales, y en algunas muestras disminuye la transmitancia, indicando que hay una disminución de los grupos funcionales y que estos interactúan habiendo más entrecruzamientos en relaciones 50/50, por lo que en esa misma relación el espesor es mayor, sin embargo, en la relación de 30/70 el espesor es menor a medida que se incrementa la nanoarcilla obteniendo una mayor área de superficie para su dispersión. Los análisis microbiológicos presentaron actividad antimicrobiana para la especie de Staphylococcus Aureus, la absorción en solución de Aloe vera presentó el triple de su peso inicial en las primeras cuatro horas, en cuanto a la permeabilidad, la muestra más permeable fue la C370, sin embargo, al aumentar la concentración de quitosano y nanoarcilla la película tiende a aumentar su permeabilidad.
Agradecimientos. Los autores externan su agradecimiento al Tecnológico Nacional de México (TecNM) por el apoyo económico recibido a través de la Convocatoria de Apoyo a la Investigación Científica y Tecnológica 2019 (Clave proyecto: 5765.19–P). K.A. Castillo–Rosales agradece al Consejo Nacional de Ciencia y Tecnología (CONACyT) por el apoyo económico para la realización de sus estudios de Maestría en Ciencias de la Ingeniería.
BIBLIOGRAFÍA
- Osorio–Delgado MA, Henao–Tamayo LJ, Velásquez–Cock JA, Cañas–Gutierrez AI, Restrepo–Múnera LM, Gañán–Rojo PF, Zuluaga–Gallego RO, Ortiz–Trujillo IC, Castro–Herazo CI, DYNA, 84(201), 241 (2017)
- Lagaron JM, Lopez–Rubio A, Trends Food Sci. Technol., 22(11), 611(2011)
- Maldonado–Lara K, Rodriguez–Herrera A, Vázquez–Álvarez FG, Hernández–Navarro C, Hernández JL “Preparación y caracterización de películas de quitosano con extractos naturales para aplicaciones biomédicas”. En Memorias del Congreso Nacional de Ingeniería Biomédica, 3(1), 165 (2017)
- Norma ASTM D 570–98, Standard Test Methods for Water Absorption of Plastics, Vol. 8.01, Filadelfia (USA): American Society for Testing and Materials, 2005
- Kim KM, Son JH, Kim SK, Weller CL, Hanna MA, J. Food Sci., 71(3), E119(2006)
- Enríquez M, Velasco R, Ortiz V, Biotecnología en el Sector Agropecuario y Agroindustrial, 10(1), 182 (2012)
- Rodriguez–Marín ML, Bello–Pérez LA, Yee–Madeira H, González–Soto RA, Rev. Mex. Ing. Quim., 12(1), 165 (2013)
- Norma ASTM D 882–02 “Standard test method for tensile properties of thin plastic sheeting”, Vol. 8.01, Filadelfia (USA), American Society for Testing and Materials, 2005
- Cissé M, Montet D, Loiseau G, Ducamp–Collin MN, J. Polym. Environ., 20(3), 830 (2012)
- Escobar–Sierra DM, Perea–Mesa YP, Dyna, 84(203), 134 (2017)
- Islam A, Yasin T, Gull N, Khan SM, Munawar MA, Shafiq M, Sabir A, Jamil T, Int. J. Biol. Macromolecules, 82(1), 551 (2016)
- Casariego ABWS, Souza BWS, Cerqueira MA, Teixeira JA, Cruz L, Díaz R, Vicente AA, Food Hydrocolloids, 23(7), 1895 (2009)
