Gabriela Lluberas*1, Gabriela Montes de Oca–Vásquez2, Diego Batista Menezes2, José R. Vega–Baudrit2,3, Pablo Raimonda4, Mary Lopretti1
1) Laboratorio de Técnicas Nucleares Aplicadas a Bioquímica y Biotecnología, Centro de Investigaciones Nucleares, UdelaR, Mataojo 2055, CP 11400, Montevideo, Uruguay. E–mail: gabriela_lluberas@hotmail.com
2) Laboratorio Nacional de Nanotecnología, Centro Nacional de Alta Tecnología, 10109 Pavas, San José, Costa Rica
3) Laboratorio de Ciencias y Tecnologías de Polímeros, Escuela de Química, Universidad Nacional, Campus Omar Dengo, 86–3000 Heredia, Costa Rica
4) Instituto de ensayo de materiales, Facultad de Ingeniería, UdelaR, Julio Herrera y Reissig 565, Código Postal 11.300
Recibido: Septiembre 2019; Aceptado: Octubre 2019
Texto completo (pdf)
Cita (APA)
Lluberas, G., Montes de Oca–Vásquez, G., Batista Menezes, D., Vega–Baudrit, J.R., Raimonda, P., Lopretti, M. (2019). Valorización de subproductos de la industrialización de aceites de soja y de la industria pesquera para la obtención de membranas poliméricas. Revista Iberoamericana de Polímeros, 20(6), 279–293.
RESUMEN
Trabajar en economía circular aumentando el valor agregado de subproductos de diferentes industrializaciones es hoy uno de los mayores temas de interés productivo. La industrialización de granos como la soja es bien conocida por la generación de subproductos, entre ellos aceites de baja calidad que pueden formularse en materiales híbridos con diversas aplicaciones. Por otro lado, los residuos sólidos de la industria camaronera generan subproductos como la quitina que puede transformarse en quitosano soluble y formar parte de nuevos materiales. El presente trabajo tuvo como objetivo optimizar la obtención de membranas, utilizando aceite de soja y quitosano, como soporte para la liberación controlada de materiales híbridos con potencial aplicación industrial. Las membranas se formularon variando la temperatura (25 y 75°C) y la agitación (200–400 rpm) obteniendo membranas con diferentes comportamientos. Las membranas se caracterizaron mediante análisis termogravimétricos (TGA), espectroscopia infrarroja transformada de Fourier (FTIR), microscopía electrónica de barrido (MEB) y ensayos físicos. De los resultados obtenidos, podemos concluir que las membranas sintetizadas, tienen las mismas propiedades químicas, pero se observan diferencias a nivel físico. Estructuralmente las membranas poseen tamaños, porosidad y resistencia, obteniendo valores interesantes dentro de las propiedades de las membranas. Este trabajo se enfocó en las características fisicoquímicas dejando para el futuro la incorporación de bioactivos y su liberación.
ABSTRACT
Working in a circular economy increasing the added value of by–products of different industrializations is today one of the major issues of productive interest. The industrialization of grains such as soybeans is well known by generating by–products including low quality oils that can be formulated in hybrid materials with various applications. On the other hand, solid waste from the shrimp industry generates by–products such as chitin that can be transformed into soluble chitosan and be part of new materials.The objective of this work was to optimize the obtaining of membranes, using soybean oil and chitosan, as a support for the controlled release of hybrid materials with potential industrial application. The membranes were formulated by varying the temperature (25 and 75°C) and agitation (200–400 rpm) obtaining membranes with different behaviors. The membranes were characterized by thermogravimetric analysis (TGA), Fourier transformed infrared spectroscopy (FTIR), scanning electron microscopy (MEB) and physical tests. From the results obtained, we can conclude that the synthesized membranes have the same chemical properties, but physical differences are observed. Structurally the membranes have adequate sizes, porosity and resistance, obtaining interesting values within the properties of the membranes. This work focused on the physicochemical characteristics leaving for the future the incorporation of bioactives and their release.
INTRODUCCIÓN
La tecnología de membranas es un área dinámica, con numerosas aplicaciones, como depuración de aguas, transportadores de diversos activos y fármacos [1–14]. Las membranas son materiales poliméricos que actúan como barrera entre dos fluidos y que restringe o favorece el movimiento de uno o más componentes de los fluidos a través de ella [15–16]. Esta definición, permite hacer una amplia clasificación de las membranas según el criterio que se escoja. Una clasificación posible toma como punto de partida cuatro enfoques distintos, su naturaleza, su estructura, su mecanismo de transferencia de materia y sus posibilidades de aplicación [17–22].
Independientemente del tipo de membrana, durante su proceso de síntesis es posible resaltar las propiedades que son más determinantes para la aplicación deseada [15–23]. Los polímeros que conforman las mismas están compuestos por una repetición ordenada de monómeros orgánicos que dan lugar a materiales de alto peso molecular con estructuras más o menos complejas. Algunas de las propiedades más características de éstos son la estereoisomería, la flexibilidad de la cadena, el peso molecular medio, las interacciones entre cadenas, el estado térmico del polímero (vidrio o goma), la cristalinidad, su estabilidad térmica y química, sus propiedades mecánicas.
Las membranas se pueden dividir en porosas y densas. Las porosas se caracterizan por tener poros fijos, que determinan su desempeño. Además, el tamaño de los poros y la distribución pueden ser factores determinantes en la selectividad, ya que controlan el paso y la velocidad de liberación de activos/sustancias [24–29]. Las membranas densas se caracterizan por la ausencia de poros estructurales, por lo tanto, el principal factor de selectividad sería el polímero utilizado en la síntesis, ya que el proceso de filtración se produce a través de ósmosis.
La naturaleza de los polímeros en membranas microporosas sólo afectará a propiedades como la adsorción física o química y la estabilidad (química, mecánica y térmica) [5–11]. Por su parte, las propiedades de transferencia de masa, para las membranas no porosas están fuertemente influenciadas por algunas de las propiedades del polímero. La elección de un polímero para una aplicación determinada depende de forma significativa de la aplicación para la cual esté destinada la membrana. Esto se debe a que las propiedades de transporte en las membranas densas (solubilidad y difusividad) dependen del material de la membrana y de la naturaleza del permeado, y sobre todo de la interacción entre ellos [21–22].
Las membranas poliméricas pueden estar fabricadas a partir de uno o varios polímeros. Recientemente las membranas basadas en los polímeros naturales, como la quitina y el quitosano, han ganado mucha atención, debido a que estos presentan características físicas, químicas y biológicas, como alta estabilidad, biocompatibilidad, baja toxicidad y biodegradabilidad, que permiten que sean atractivas como membranas de soporte con potenciales aplicaciones como vehículo y liberación de una gran variedad de activos [23–25].
Las membranas también pueden sintetizarse por emulsión. Sin embargo, estos sistemas formados por líquidos inmiscibles se consideran termodinámicamente inestables, siendo el polímero la fase continua y la emulsión la fase dispersa. Las partículas del líquido dividido se encontrarán formando la fase dispersa y el líquido en el cual estas gotas están dispersas será el formador de la fase continua [24–28].
Una fase estará constituida por una sustancia acuosa y la otra por una sustancia oleosa, debido a esto hay dos clases de emulsiones, agua en aceite W/O donde la fase dispersa es el agua y aceite en agua O/W donde la fase dispersa es la oleosa. Muchas veces se puede transformar una emulsión W/O en O/W, o a la inversa, por pequeñas modificaciones en el sistema, fenómeno denominado “inversión”. Debido a la tensión superficial de las gotas el sistema posee una estabilidad mínima que puede ser controlada añadiendo un tensoactivo o emulsificante [26–29].
Este trabajo se basó en el desarrollo de membranas de quitosano con potencial aplicación para la incorporación y liberación de bioactivos de interés industrial. Se utilizó quitosano de crustáceo como biopolímero, obtenido por desacetilación química de la quitina, para la síntesis de la matriz de membranas. Las membranas se prepararon utilizando una metodología basada en la preparación de una emulsión agua en aceite (w/o) seguida de entrecruzamiento o no con glutaraldehído. La caracterización de los sistemas obtenidos, se realizaron por microscopía electrónica de barrido, estudios termogravimétricos, mecánicos, liberación controlada y absorción de agua.
METODOLOGÍA
Materiales: El quitosano (grado de desacetilación del 95%) se obtuvo según la metodología descrita por Lopretti et al. [27], que consistió en la desacetilación de la quitina y la solubilización de la misma en ácido acético. El glutaraldehído y el alcohol polivinílico, utilizados fueron de grado analítico, se utilizó aceite de soya comercial (Cousa, Uruguay). Para preparar las disoluciones se utilizó agua desionizada.
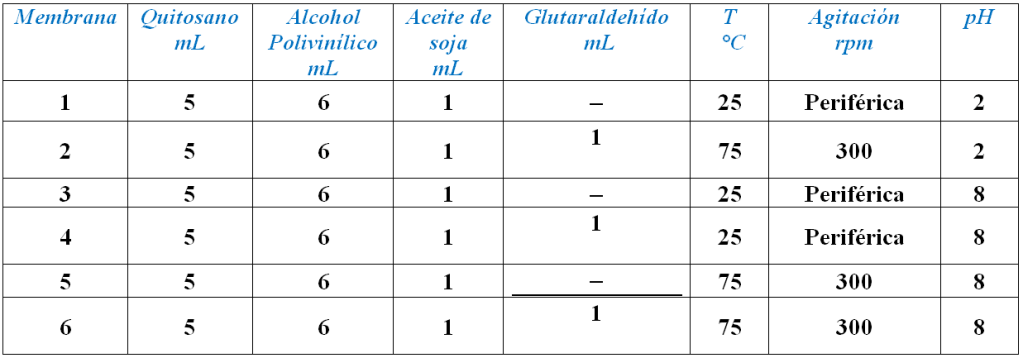
Síntesis de las membranas de quitosano: Para la preparación de las membranas, se utilizó como fase dispersa una solución de quitosano al 1,0% (w/v) en ácido acético al 5% y se filtró utilizando papel con una porosidad de 11 μm. Para la fase continua, se tomó 150 mL de aceite de soja en un matraz de 500 mL. Se le adicionó 0,1% (w/w) de Span 80. Utilizando una jeringa, se agregaron 5 mL de la solución quitosano 1,0% por goteo (5 mL min–1) sobre el aceite de soja, con agitación constante a 300 rpm o agitación periférica, y a temperatura ambiente (25°C) y/o 75 °C. Posteriormente se agregó glutaraldehído y/o alcohol polivinílico los cuales se adicionaron a pH 2 y 8, manteniendo la agitación constante, según las condiciones descritas en la tabla I. Una vez agregado el alcohol polivinílico, se mantuvieron las mismas condiciones de agitación durante una hora. Se introduce la emulsión en el molde y se procede al secado en estufa a 30°C por 24 horas. Las membranas se realizaron por triplicado.
Caracterización de las membranas de quitosano. Análisis infrarrojo por transformada de Fourier (FTIR). Con el fin de determinar los principales grupos funcionales de las membranas de quitosano, y sus materiales de partida, se llevó a cabo el análisis infrarrojo por transformada de Fourier (FTIR). Los espectros FTIR se recolectaron a una resolución de 1 cm−1 en el modo de transmisión (4.000–500 cm−1) utilizando un espectrofotómetro FTIR (Nicolet 6700, Thermo Scientific). Los análisis se realizaron por duplicado.
Análisis termogravimétrico (TGA). La determinación de la temperatura de degradación se realizó mediante la técnica de análisis termogravimétrico (TGA). Se utilizaron 5 mg de muestra, y una rampa de temperatura de 20°C/min desde 40 a 700°C bajo nitrógeno (flujo de 90 mL/min), utilizando un equipo Q500 (TA Instruments, USA.). Se analizaron todas las membranas de quitosano, además de los materiales de partida, como el quitosano, aceite de soja y glutaraldehído. Los análisis se realizaron por duplicado.
Microscopía electrónica de barrido (SEM): Las membranas fueron observadas a través de un microscopio electrónico de barrido (Jeol, modelo JSM 5900 LV), equipado con EDS. Los análisis se realizaron bajo una aceleración de voltaje de 20 KV, SEI y tamaño de punto: 50. Las muestras se recubrieron con una capa muy fina de oro en una cubierta iónica EMS 550X Sputter Coater a 50 mA durante 2:30 minutos con un vacío de 1·10–1 mbar.
Ensayos de liberación de colorante en medio acuoso. Se realizaron ensayos de liberación en medio acuoso, de todas las membranas desarrolladas. Para el mismo, se les agregó 500 mL de una solución 1% de azul de metileno B (Anedra, lote 4726). Luego se procedió a la inmersión de una porción de membrana de 1 cm3 en un medio acuoso a temperatura ambiente durante 7 días. Se tomaron muestras del medio acuoso, diariamente, las cuales se midieron en un espectrofotómetro UV–1800 (Evolution 160 UV–Vis, Thermo Scientific) en un rango entre 640 a 660 nm. Se realizó una curva de calibración a partir de una solución madre de 0,25 mg/mL, se realizaron diluciones hasta tener un intervalo de concentraciones cuya absorbancia a 650 nm (máximo de absorción) fuera mayor a 0,1 y menor a 1.
Ensayo de tracción: Se realizó en una máquina universal de ensayos, marca Instron, modelo 1011, a una velocidad de 10 mm/min. Las condiciones de ensayo fueron 20°C y 44% de HR. Los ensayos se realizaron por triplicado.
Ensayo de absorción y desorción de agua: El porcentaje de absorción de agua se determinó por pesada en balanza analítica, sumergiendo la probeta durante 24 horas en agua destilada. Se determinó el peso inicial y final de las membranas después de las 24 horas. Mientras que para la desorción se realizó por pesada luego de secar la misma a 90°C durante 48 horas. El ensayo se realizó a una temperatura de 20°C, 36% HR. Los análisis se realizaron por triplicado.
RESULTADOS
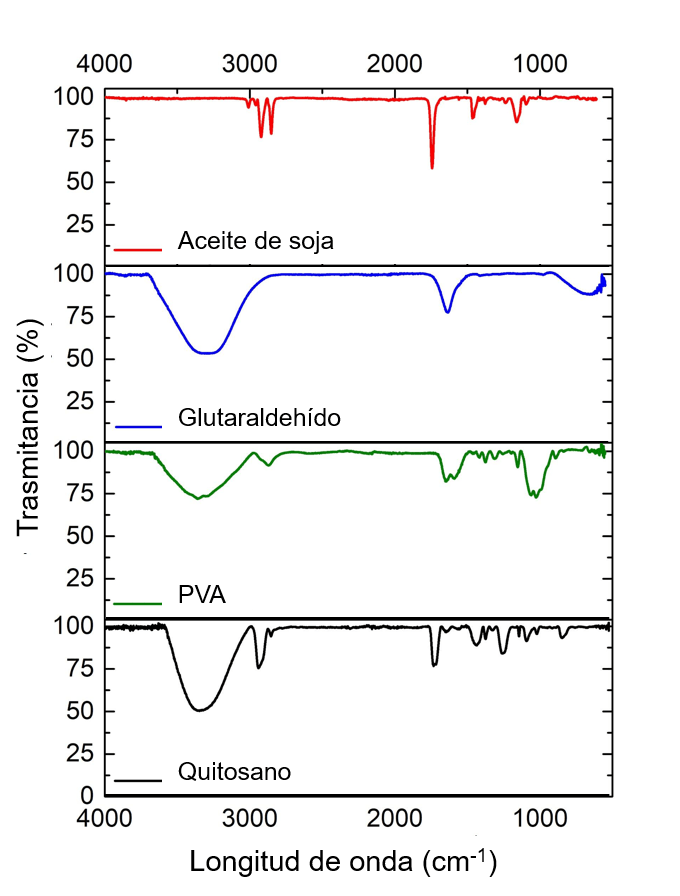
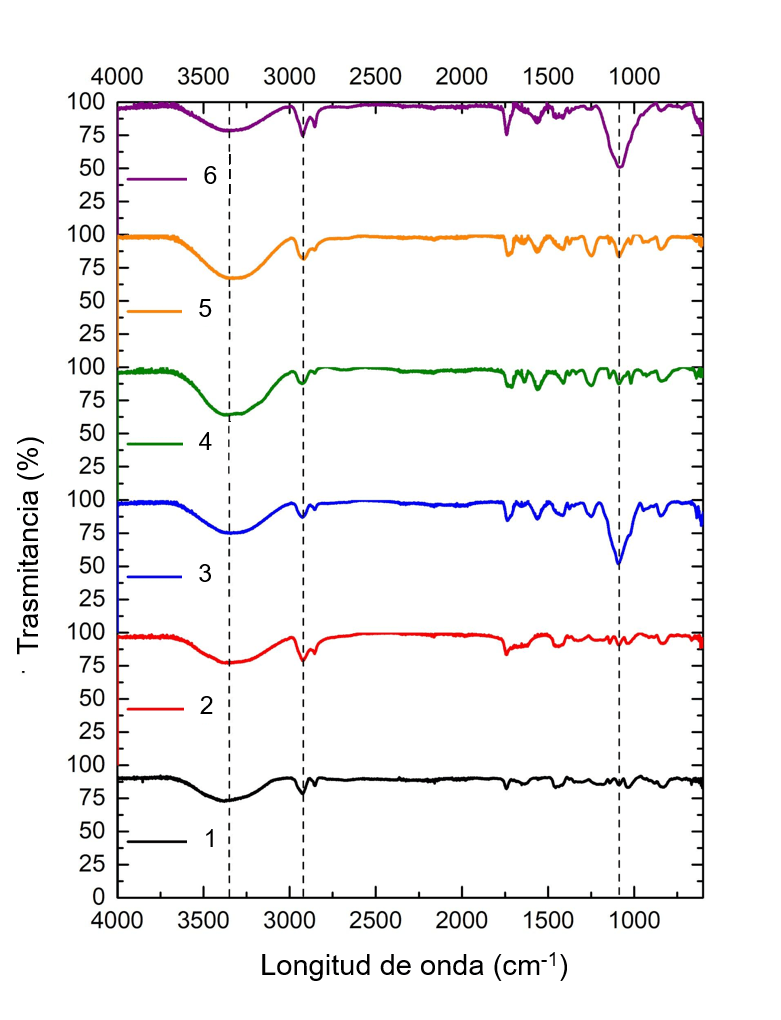
Espectroscopia Infrarroja: Los espectros infrarrojos de los materiales de partida se observan en la Figura 1. Se encontraron las señales típicas de los distintos materiales. Los espectros infrarrojos de los films se observan en la Figura 2. Se puede determinar que el grado de humedad en las membranas es muy similar entre sí, esto se aprecia gracias a la señal cerca de 3.330 cm–1, correspondiente al estiramiento del enlace O–H de la molécula de agua. Esta señal tiene una forma e intensidad similar en todas las muestras. Cerca de 2.920 cm–1 se observa la señal correspondiente al estiramiento del enlace C–H de los alcanos. En este caso específico esta señal se asigna al quitosano, alcohol polivinílico, glutaraldehido y aceite de soja.
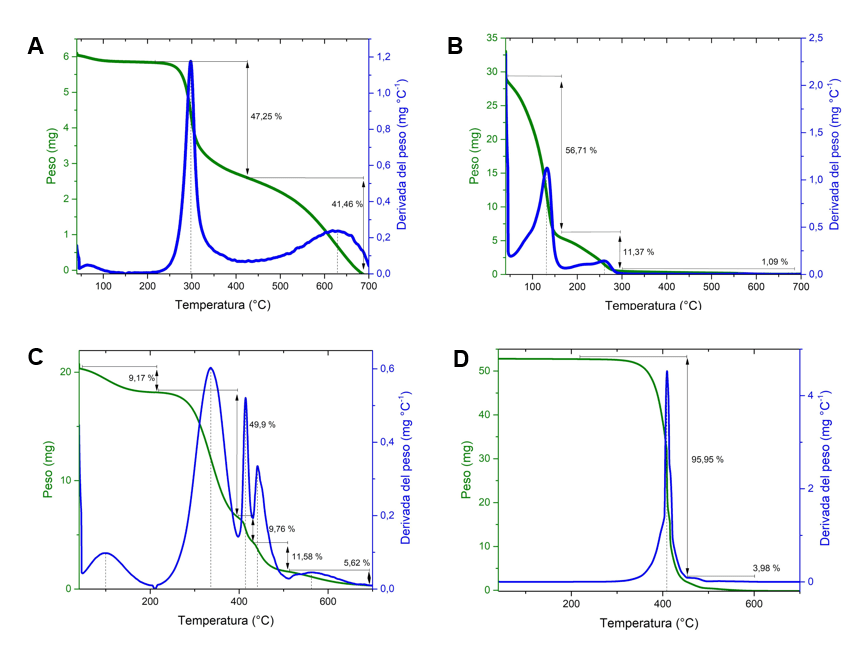
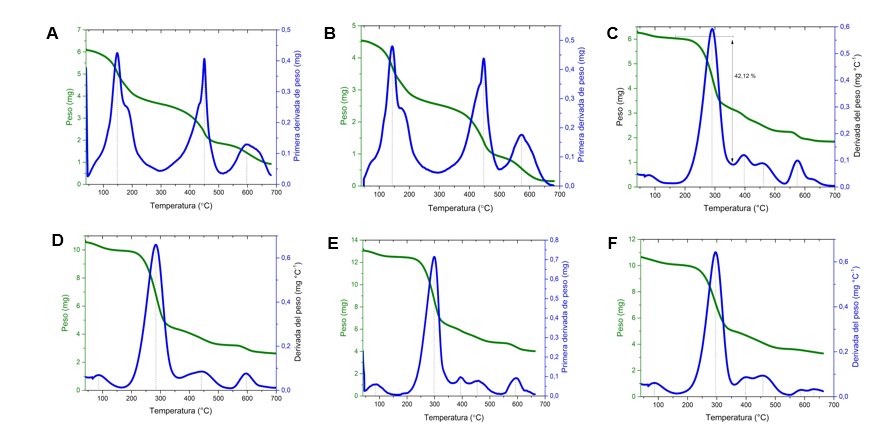
Análisis termogravimétricos (TGA): En la Figura 3 se muestran los análisis de TGA del quitosano, glutaraldehído, PVA y aceite de soja. En el caso del quitosano (Figura 3A) se observa una pérdida de masa a una temperatura menor a 150°C, además, cerca de 300°C se observa otra pérdida de masa, alrededor del 47%. La tercera pérdida de masa se observa entre 500 y 700°C, se puede determinar una señal muy paulatina, que abarca el 41% de la masa. La Figura 3B muestra la descomposición del glutaraldehido, la cual ocurre por debajo de 300°C. A temperaturas menores a 150°C se presenta una gran desorción de agua. Al igual que los componentes anteriormente mencionados, en el TGA del PVA (Figura 3C) se observa una señal a los 100°C con una pérdida de un 9% de la masa. A una temperatura mayor a 300 °C se da otra pérdida abrupta de masa. Seguidamente, aparecen dos pérdidas de masa cerca de los 400°C, con un porcentaje de pérdida de un 49,9 y un 9,76%, respectivamente. Por último, se determinó una pérdida de masa por arriba de 500°C. En el aceite de soja (Figura 3D) solo se observa una señal muy cerca de 400°C, lo cual representa un 96% de la muestra.
Los resultados para los análisis termogravimétricos (TGA) de las membranas se muestran en la Figura 4. Las membranas 1 y 2 presentan pérdidas de masa, muy similares, que se observan de 150 y 450°C. Sin embargo, en la membrana 1, a diferencia de la 2, se encontró una pérdida de masa a los 500°C, y en la 2 a los 550°C. Por su parte, la membrana 3, 4, 5 y 6 fueron similares entre sí, pero muestran una composición muy distinta a las 2 y 3, ya que la mayor pérdida de masa se da a los 300°C, con otras pérdidas menores, cercanas a los 400, 450, y 575 a 600°C.
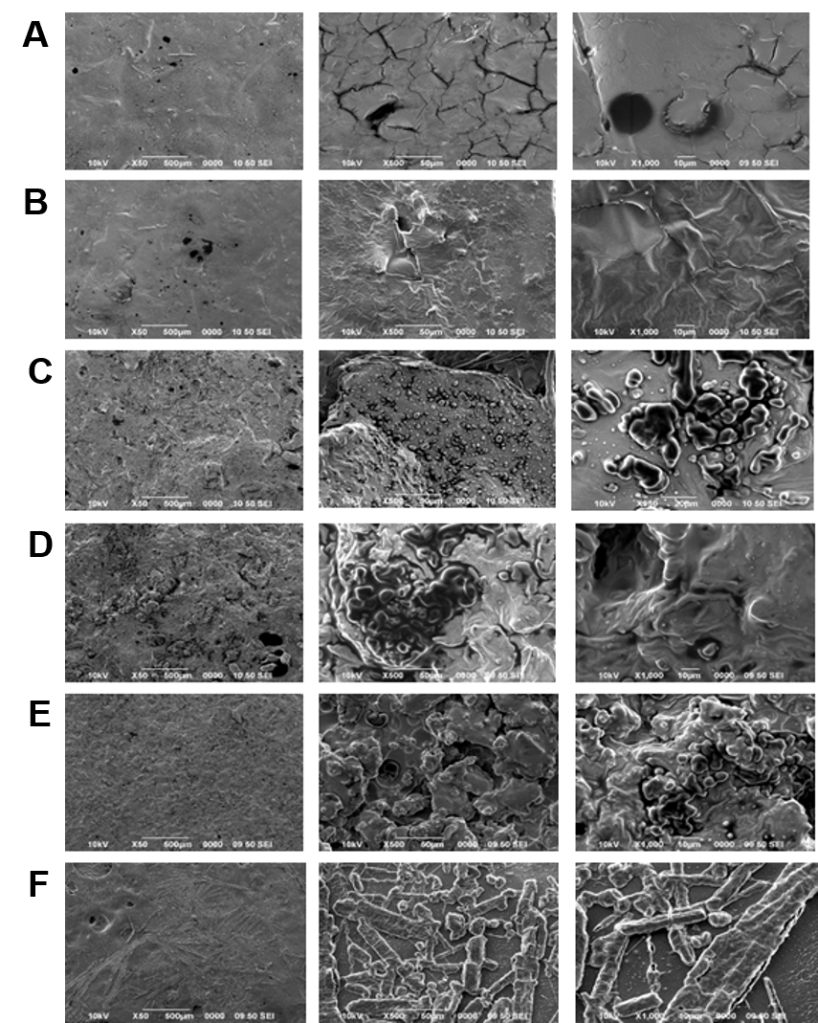
Microscopía electrónica de barrido. En la Figura 5 se observan las micrografías electrónicas de barrido de la superficie de las distintas membranas sintetizadas. Los análisis de SEM muestran diferencias principalmente entre las membranas sintetizadas a pH ácido y básico. Las de pH ácido, tuvieron una morfología más lisa, comparado con las de pH básico que presentan una superficie rugosa. La membrana 1, presenta una superficie lisa con algunas rupturas, sin embargo, la membrana 2, presenta una superficie lisa con algunos pliegues, sin la presencia de rupturas. Por su parte, la membrana 3 al igual que la 5, presentan una superficie rugosa con formación de gránulos. La membrana 4 posee morfología en forma de roseta. Por su parte, la 6, presenta en su superficie unas estructuras tubulares distribuidas de forma irregular.
Ensayos de liberación de colorante en medio acuoso. Se procedió a la evaluación de liberación del colorante Azul de metileno según la metodología descrita anteriormente (2.4), a partir de la misma se logró obtener la Figura 6 mostrada a continuación.
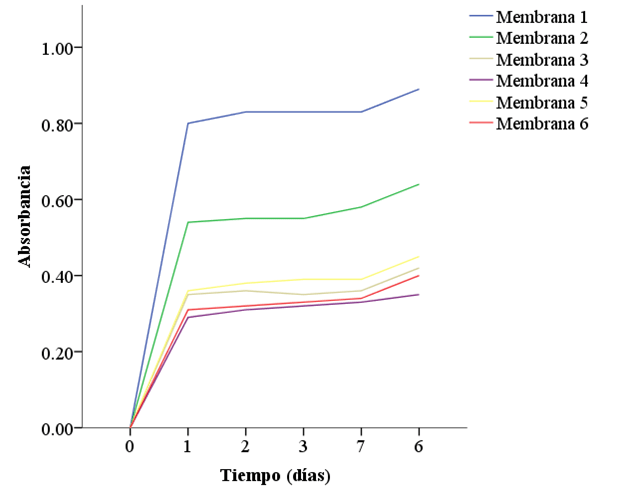
A partir de la Figura 6 se puede ver que las membranas tienen una amplia diferencia en la liberación del colorante utilizado. Esto juega un papel muy importante ya que dependiendo del uso final de la membrana una rápida o una liberación sostenida es que se elige la metodología de síntesis de esta. Se determinó que las membranas que en su constitución no poseen glutaraldehido como entrecruzante y poseen pH ácido tienen una mayor liberación.
Cabe recalcar, la importancia que tiene el pH en las membranas, ya que a un pH ácido el quitosano tiene una mayor solubilidad que en un medio alcalino, y las membranas 1 y 2 fueron sintetizadas en un medio ácido y son las que tienen una liberación más pronunciada y rápida que las sintetizadas en un medio alcalino.
Propiedades mecánicas: Las propiedades mecánicas de las membranas, fueron determinadas tal cual se establece 2.2.4, y se resumen en la Tabla II.
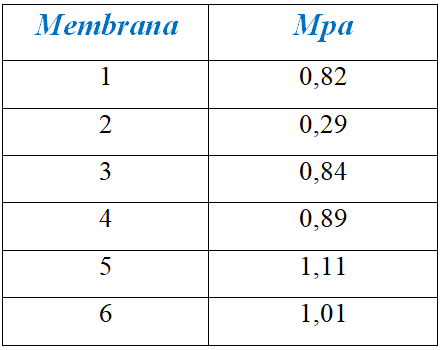
Como se desprende de la misma, las membranas producidas en medio básico y con buena agitación son las que presentan mejores propiedades mecánicas. Más aún, si se comparan en su totalidad todos los datos obtenidos en la tabla II, vemos que la variable que más influencia este tipo de propiedades es la agitación. Por último, si se observan, los resultados obtenidos para las membranas 5 y 6, se aprecia claramente la influencia del agente de entrecruzamiento, el glutaraldehído, en conjunto con la temperatura, cuyo objetivo es obtener una estructura más rígida. A bajas temperaturas, (membranas 3 y 4), el efecto del reticulante no es tan marcado.
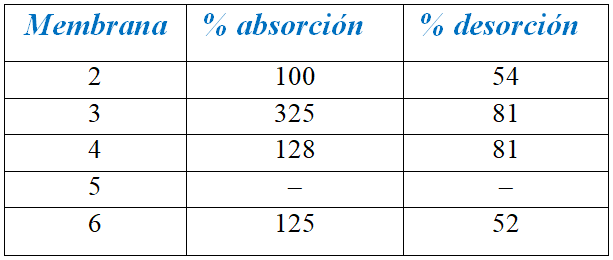
En lo que hace a la absorción de agua, bajo las condiciones de ensayo, observamos que independientemente de las condiciones de preparación de las membranas, los resultados son similares, a excepción de la membrana 3, que es capaz de adsorber aproximadamente el triple que el resto, resultado que para su explicación requiere de más ensayos.
DISCUSIÓN
Las membranas se realizaron a partir de cuatro componentes principales, quitosano, PVA, aceite de soja y glutaraldehído. Los análisis de TGA de estos componentes, muestran diferencias entre sí. En el caso del quitosano se observa una pérdida de masa a temperaturas menores a 150°C, dada la forma de señal y la temperatura, se puede atribuir esta pérdida a la desorción de agua en la muestra. Si comparamos estos datos con las mediciones realizadas a 90°C, por el método tradicional, (ver tabla III), determinamos que no todo lo que se observa en el TGA a 150°C es agua. Mayores ensayos, con un TGA adosado a un FTIR, nos podrían indicar la composición real en esta zona de las curvas, dando mejores resultados sobre el comportamiento térmico de estos productos.
A los 300°C se observa la mayor y más brusca pérdida de masa, alrededor de 47%. Es muy común tener una pérdida grande de masa alrededor de estas temperaturas, lo cual depende del grado de desacetilación de la muestra. Según se ha reportado, en esta pérdida se libera una compleja mezcla de gases, CO, CO2, NH3, H2O, CH4 y CH3COOH. La misma se asocia con la pirólisis del quitosano. La tercera pérdida de masa de la curva se observa entre 500 y 700°C, se puede observar una señal muy paulatina, que abarca el 41% de la masa. Según reportan Corazzari et al, la misma corresponde a una liberación de metano, lo cual se puede asociar con pequeños cambios estructurales cuando la mayor parte de la estructura del quitosano se ha reducido. Con respecto a la descomposición del glutaraldehído, ocurre por debajo de 300 °C. A temperaturas menores a 150 °C se presenta una gran desorción de agua, ya que el glutaraldehído no se encuentra puro. Con respecto al TGA del PVA, se observa una señal cerca de 100 °C que se atribuye al fenómeno de desorción de agua, cerca de 9 % de la masa de la muestra se pierde. A una temperatura mayor a 300°C se observa una pérdida abrupta de masa, asociado con el fenómeno de eliminación de grupos hidroxilo, formando dobles enlace de carbono en la cadena, lo cual resulta en la liberación de agua. Seguidamente, aparecen dos pérdidas de masa que se relacionan en general con la descomposición de grupo carbonilo y de dobles enlaces en la estructura conjugada. Por último, observa una pérdida de masa por arriba de 500°C, que se debe a la remanencia de pequeñas estructura modificadas provenientes de la previa descomposición.
El aceite de soja (fig. 3D) se observa prácticamente sólo una señal muy cerca de 400°C, esto representa un 96% de la muestra, en esta señal se observan hombros correspondientes a distintas descomposiciones dado la variada descomposición del aceite de origen natural.
Los espectros infrarrojos de los films de quitosano, determinaron que el grado de humedad en las membranas es muy similar entre sí, esto se aprecia gracias a la señal cerca de 3.330 cm–1, correspondiente al estiramiento del enlace O – H de la molécula de agua. Esta señal tiene una forma e intensidad similar en todas las muestras. Además, cerca de 2.920 cm–1 se observa la señal correspondiente al estiramiento del enlace C – H de los alcanos. En este caso específico la misma es asignada al quitosano, alcohol polivinílico, glutaraldehido y aceite de soja.
También debemos considerar el pH utilizado en la síntesis de las membranas, esto es importante debido a que a pH ácido la solubilidad del quitosano se ve aumentada respecto a un pH básico modificando así la disponibilidad de este en las membranas, siendo esto un factor muy importante a considerar ya que influye sobre las propiedades físicas de las membranas.
Cabe destacar que a nivel químico no se observan diferencias significativas entre las membranas, pero si se ven características bien variadas a nivel físico y de liberación de compuestos retenidos en las mismas. Podemos concluir a partir del ensayo de liberación realizado las membranas que poseen glutaraldehído van a tener una liberación más controlada respecto a las que poseen solo PVA y a su vez las membranas sintetizadas en un pH ácido van a tener una liberación más rápida que las sintetizadas en un medio alcalino.
Con respecto a las propiedades físicas, el ensayo de tracción nos muestra que el pH al que se obtienen las membranas tiene una marcada influencia en las propiedades mecánicas del producto final obtenido, tal cual se desprende de la tabla II, A su vez, a pH ácido un aumento de la temperatura es perjudicial para este tipo de propiedades, como se observa en el caso de la membrana 2. Por otra parte, contrariamente a lo que se esperaría, la acción reticulante del glutaraldehído, no posee influencias marcadas sobre las propiedades mecánicas, al comparar las resistencias a la tracción de las membranas número 5 y 6, las cuales se diferencian únicamente en la presencia o no de glutaraldehído. Por último, otra de las propiedades interesantes a estudiar en este tipo de productos es su facilidad para la absorción o liberación del solvente en el que se sumergen, agua en nuestro caso de estudio. Bajo a este aspecto, las membranas que contienen glutaraldehído, son las que absorben más agua, y retienen menos, lo que de alguna manera podría estar facilitando la liberación más controlada de productos, hipótesis que debe corroborarse con otro tipo de experimentos.
CONCLUSIONES
A partir de esta investigación se puede concluir que el material híbrido obtenido a partir de quitosano, alcohol polivinílico, glutaraldehído y aceite de soja permite obtener membranas con buena resistencia y entrecruzamiento adecuado para que retenga diferentes bioactivos y con buena propiedad mecánica.
A partir del ensayo de liberación realizado las membranas que poseen glutaraldehído van a tener una liberación más controlada respecto a las que poseen solo PVA y a su vez las membranas sintetizadas en un pH ácido van a tener una liberación más rápida que las sintetizadas en un medio alcalino. Estas diferencias permiten con la misma matriz obtener soportes para múltiples usos tanto en el agro, como en tratamiento de efluentes, usos veterinarios etc.
BIBLIOGRAFÍA
1. Wang, L. Z., Gorlin, J., Michaud, S. E., Janmey, P. A., Goddeau, R. P., Kuuse, R., … & Sawyer, E. S. (2000). Purification of salmon clotting factors and their use as tissue sealants. Thrombosis research, 100(6), 537-548.
2. Martínez Álvarez, Ó. (2011). Estado actual del aprovechamiento de subproductos de la industria pesquera mediante la obtención de productos de alto valor añadido. Alimentaria: Revista de tecnología e higiene de los alimentos, 429, 71– 80.
3. Casis, N., Fidalgo, M. M., Ravaine, S., & Estenoz, D. A. (2010). Elaboración de membranas poliméricas porosas a partir de cristales coloidales. Información tecnológica, 21(1), 3-8.
4. Méndez-Durán, A., Méndez-Bueno, J. F., Tapia-Yáñez, T., Montes, A. M., & Aguilar-Sánchez, L. (2010). Epidemiología de la insuficiencia renal crónica en México. Diálisis y trasplante, 31(1), 7-11.
5. Ávila-Saldivar, M. N., Conchillos-Olivares, G., Rojas-Báez, I. C., Ordoñez-Cruz, A. E., & Ramírez-Flores, H. J. (2013). Enfermedad renal crónica: causa y prevalencia en la población del Hospital General La Perla. Med Interna México, 473-478.
6. Méndez-Durán, A., Pérez-Aguilar, G., Ayala-Ayala, F., Ruiz-Rosas, R. A., de Jesús González-Izquierdo, J., & Dávila-Torres, J. (2014). Panorama epidemiológico de la insuficiencia renal crónica en el segundo nivel de atención del Instituto Mexicano del Seguro Social. Diálisis y Trasplante, 35(4), 148-156.
7. Yamashita, A. C., & Sakurai, K. (2015). Dialysis membranes–physico-chemical structures and features. Updates in Hemodialysis; Suzuki, H., Ed.; INTECH: Vienna, Austria, 163-189.
8. Krueger, K., Terne, C., Werner, C., Freudenberg, U., Jankowski, V., Zidek, W., & Jankowski, J. (2013). Characterization of polymer membranes by MALDI mass-spectrometric imaging techniques. Analytical chemistry, 85(10), 4998-5004.
9. Amiji, M. M. (1995). Permeability and blood compatibility properties of chitosan-poly (ethylene oxide) blend membranes for haemodialysis. Biomaterials, 16(8), 593-599.
10. Abe, Y., & Mochizuki, A. (2003). Hemodialysis membrane prepared from cellulose/N‐methylmorpholine‐N‐oxide solution. II. Comparative studies on the permeation characteristics of membranes prepared from N‐methylmorpholine‐N‐oxide and cuprammonium solutions. Journal of applied polymer science, 89(2), 333-339.
11. Ethève, J., Déjardin, P., & Boissière, M. (2002). Influence of pH on the adsorption of lysozyme on a sulfonated membrane with and without poly (ethyleneimine). Desalination, 146(1-3), 111-113.
12. Lee, K. H., Kim, D. J., Min, B. G., & Lee, S. H. (2007). Polymeric nanofiber web-based artificial renal microfluidic chip. Biomedical microdevices, 9(4), 435-442.
13. Hayama, M., Yamamoto, K. I., Kohori, F., & Sakai, K. (2004). How polysulfone dialysis membranes containing polyvinylpyrrolidone achieve excellent biocompatibility?. Journal of membrane science, 234(1-2), 41-49.
14. Wang, Z. G., Wan, L. S., & Xu, Z. K. (2007). Surface engineerings of polyacrylonitrile-based asymmetric membranes towards biomedical applications: An overview. Journal of Membrane Science, 304(1-2), 8-23.
15. Park, J. Y., Acar, M. H., Akthakul, A., Kuhlman, W., & Mayes, A. M. (2006). Polysulfone-graft-poly (ethylene glycol) graft copolymers for surface modification of polysulfone membranes. Biomaterials, 27(6), 856-865.
16. Schulze, R. D., Possart, W., Kamusewitz, H., & Bischof, C. (1989). Young’s equilibrium contact angle on rough solid surfaces. Part I. An empirical determination. Journal of adhesion science and technology, 3(1), 39-48.
17. Malamud, D., & Drysdale, J. W. (1978). Isoelectric points of proteins: a table. Analytical biochemistry, 86(2), 620-647.
18. Kamide, K., & Manabe, S. I. (1980). Characterization technique of straight-through porous membrane. In Ultrafiltration Membranes and Applications (pp. 173-202). Springer, Boston, MA.
19. Rasneur, B. (1984). Porosimetry (characterization of porous membranes). In Summer School on Membrane Sci. and Tech.. Cadarache France.
20. Lowell, S., & Shields, J. E. (1991). Powder surface area and porosity (Vol. 2). Springer Science & Business Media.
21. Palacio Martínez, L. (1999). Caracterización estructural y superficial de membranas microporosas. Tesis Doctoral, Universidad de Valladolid (España).
22. Sakanaka, L. S. (2000). Efecto de las Interacciones entre Proteínas sobre el Potencial Zeta a Diversos pH y Fuerzas Iónicas. In Coloides e interfases: estado líquido (pp. 215-228). Servicio de Publicaciones.
23. Persson, K. M., & Nilsson, J. L. (1991). Fouling resistance models in MF and UF. Desalination, 80(2-3), 123-138.
24. Jönsson, C., & Jönsson, A. S. (1995). Influence of the membrane material on the adsorptive fouling of ultrafiltration membranes. Journal of Membrane Science, 108(1-2), 79-87.
25. Chang, I. S., & Kim, S. N. (2005). Wastewater treatment using membrane filtration—effect of biosolids concentration on cake resistance. Process Biochemistry, 40(3-4), 1307-1314.
26. Calvo-Brenes, G., Mora-Molina, J., Quesada-Kimsey, J., & Quesada-Carvajal, H. (2011). Aplicación de la tecnología de membranas en el tratamiento de algunos residuos líquidos altamente peligrosos. Revista Tecnología En Marcha, 23(1), 94.
27. Lopretti, M. I. Olazabal, L. (2014). Microencapsulación de microorganismos Kluyveromyces marxianus en diferentes sistemas y materiales. Evaluación de su actividad biológica en la producción de bioetanol a partir de materiales lignocelulósicos. Revista iberoamericana de polímeros, 15(1) 55-65.
28. Rootare, H. M., & Prenzlow, C. F. (1967). Surface areas from mercury porosimeter measurements. The Journal of physical chemistry, 71(8), 2733-2736.
29. Aranberri, I., Binks, B.P., Clint, J.H., Fletcher, P.D.I. (2006). Elaboración y caracterización de emulsiones estabilizadas por polímeros y agentes tensoactivos, Revista iberoamericana de polímeros, 7(3), 211-231.
30. Rustad, T., Storrø, I., & Slizyte, R. (2011). Possibilities for the utilisation of marine by‐products. International Journal of Food Science & Technology, 46(10), 2001-2014.
