Ilse Paulina Verduzco Navarro1, Daniel Álvarez Vázquezb, Sergio Iván Yáñez Barragánb, Carlos F. Jasso–Gastinel, Nely Ríos–Donatoa, Eduardo Mendizábala*
1) Departamento de Química, CUCEI, Universidad de Guadalajara, Jalisco, 44430, México. Correo electrónico: lalomendizabal@hotmail.com / eduardo.mmijares@academicos.udg.mx
2) Departamento de Ingeniería Química, CUCEI, Universidad de Guadalajara, Jalisco, 44430, México
Recibido: Agosto 2019; Aceptado: Octubre 2019
Texto completo (pdf)
Cita (APA)
Verduzco Navarro, I. P., Álvarez Vázquez, D., Yáñez Barragán, S. I., Jasso–Gastinel, C. F., Ríos–Donato, N., Mendizábal, E. (2019). Remoción de colorante Rojo 40 mediante percolación en columnas empacadas con hidrogeles de alginato–quitosano. Revista Iberoamericana de Polímeros, 20(6), 246–254.
RESUMEN
Se prepararon hidrogeles de alginato (Alg) – quitosano (Q) en forma de perlas para empacar columnas de percolación. Las columnas se usaron para remover colorante Rojo 40 de disoluciones acuosas; se estudió el efecto de la velocidad de flujo, la concentración inicial de colorante y la altura del lecho. Se encontró que al aumentar la velocidad de flujo, la capacidad de remoción de la columna disminuyó y que al aumentar la concentración inicial de colorante, se aumentó la capacidad de remoción de la columna. Al utilizar una altura de lecho menor se obtuvo una menor capacidad de remoción. Se observó un significante aumento en el pH de las soluciones de colorante a la salida de la columna comparado con el pH (5,0) de la solución a la entrada, lo cual se atribuye a la transferencia de protones de la solución a los grupos amino de la quitosana. Después del punto de ruptura, las columnas continúan removiendo cantidades considerables de colorante. No se alcanzó la saturación de las columnas aún después de 150 horas de operación.
ABSTRACT
Alginate (Ala)–Chitosan (Q) hydrogels were prepared in the form of pearls to pack percolation columns. The columns were used to remove Red 40 dye from aqueous solutions; the effect of flow rate, initial dye concentration, and bed height was studied. It was found that as the flow rate increased, the removal capacity of the column decreased, and as the initial dye concentration increased, the removal capacity of the column increased. Using a lower bed height resulted in lower removal capacity. A significant increase in pH was observed at the exit of the column, compared with the pH (5,0) of the dye solution at the entrance; which is attributed to the transfer of protons from the solution to the amino of the chitosan. After the breaking point, the columns continue to remove considerable amounts of dye. Saturation of the columns was not reached even after 150 hours of operation.
INTRODUCCIÓN
La contaminación con colorantes de los cuerpos de agua receptores de las aguas residuales causa efectos extremadamente tóxicos a la vida acuática aún a bajas concentraciones [1]. Existen varias tecnologías propuestas para la eliminación de colorantes del agua tales como: separación por membrana [2], extracción líquido–líquido [3], coagulación química y electrocoagulación [4], adsorción [5], entre otras. La adsorción es un método muy utilizado por su diseño simple, es fácilmente aplicable e implica bajos costos de operación [6–8].
A pesar de que el carbón activado es un adsorbente universal bastante efectivo, su uso generalizado en el tratamiento de aguas se encuentra restringido por su alto costo, por lo que la adsorción utilizando adsorbentes de bajo costo es un método efectivo y económico para la limpieza de aguas [9]. El quitosano (Q) puede ser utilizado como un adsorbente afectivo para la remoción de colorantes debido a la presencia de grupos amino e hidroxilo, los cuales pueden servir como sitios activos [7,10]. Es difícil utilizar el quitosano en polvo o escamas para empacar columnas debido a sus características (densidad, forma y tamaño), ya que esto ocasionaría problemas en el sistema de adsorción mediante percolación en columna, tales como caída de la presión hidrodinámica o la obstrucción de la columna [11,12].
La utilización de adsorbentes dispersos en hidrogeles en forma de perlas permite su aplicación en columnas de percolación y se tiene la ventaja de su reutilización [13]. El alginato (Ag) es útil en la obtención de hidrogeles entrecruzados para la remoción de colorantes [14]. Recientemente se ha reportado el uso de hidrogeles de alginato–quitosano (Alg-Q) en forma de perlas para la remoción de Rojo 40 en sistemas por lotes [15]. En este contexto, en este estudio se evaluó la utilización de columnas empacadas con hidrogeles de Alg-Q para la remoción de Rojo 40 en sistemas operados en continuo.
PARTE EXPERIMENTAL
Obtención y caracterización de las perlas de Alg-Q. Se añadió quitosano en polvo (América Alimentos, México) a una disolución acuosa de alginato de sodio (Sigma Aldrich, Reino Unido) al 1,5% m/m. La suspensión se colocó en un frasco, el cual se conectó al encapsulador Büchi Modelo 390 y se obtuvieron las perlas al pasar la suspensión a través de una boquilla de 1.000 µm de diámetro a 250 mBar y una frecuencia de 600 Hz. Se recolectaron las perlas en una disolución acuosa de CaCl2 (Fermot, México) 0,1 M, donde permanecieron durante 6 horas para su endurecimiento. Posteriormente, se lavaron y almacenaron en agua bidestilada.
El contenido de Q en el hidrogel se determinó utilizando la metodología descrita por Verduzco–Navarro et al. [15], utilizando citrato de sodio (Fermont, México) 0,1 M. El contenido de humedad se determinó por gravimetría. El tamaño promedio de las perlas se determinó midiendo 100 perlas con un Vernier Digital Scala. La morfología de las perlas se observó mediante un microscopio digital GAOSUO.
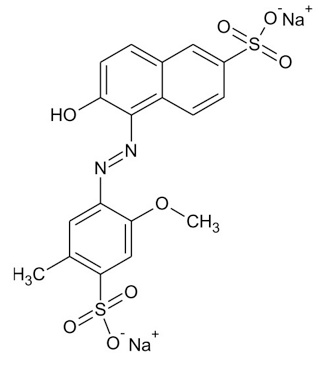
Pruebas de adsorción de Rojo 40. Se preparó una disolución de 1 g·L–1 de Rojo Allura E–123 (colorante Rojo 40, Figura 1) en agua bidestilada, con la cual se prepararon disoluciones de 10 y 20 mg·L–1. El pH se ajustó a 5,0 con una disolución de HCl 0,1 M. Se utilizaron columnas de vidrio con un diámetro interno de 1,8 cm y altura de 13 y 33 cm. Para la alimentación de las columnas con disolución de colorante se utilizaron mangueras de silicón Masterflex L/S 14 y una bomba peristáltica Masterflex 07557. La concentración de Rojo 40 en las muestras de alimento y efluente se determinó mediante lecturas en un espectrofotómetro UNICO modelo 1.000 a una longitud de onda de 500 nm. Se obtuvo una curva de calibración de Rojo 40 para determinar la concentración del colorante en las muestras.
La capacidad de adsorción de la columna (qi) a un tiempo i fue determinada mediante la ecuación 1:
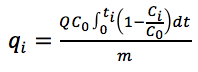
donde Q corresponde a la velocidad de flujo (L·h–1), C0 es la concentración de colorante a la entrada de la columna (mg·L–1), Ci es la concentración de colorante a la salida de la columna, m corresponde a la masa del adsorbente en la columna (g) y t representa el tiempo (h). Se consideró que el tiempo de ruptura tb se alcanzó cuando la razón entre la concentración a la salida de la columna fue equivalente al 10% del valor de la concentración a la entrada.
RESULTADOS Y DISCUSIÓN
Caracterización de las perlas. Las perlas de Alg-Q presentaron una morfología cuasi–esférica (Figura 2) y un diámetro promedio de 2,1 ± 0,3 cm. Se determinó que los hidrogeles contenían 3,0% alginato, 2,5% quitosano y 94,5% de humedad.

Adsorción de Rojo 40 por las columnas. En la Tabla 1 se resumen los datos obtenidos de las pruebas de adsorción en las columnas de percolación. En la tabla se reporta el tiempo de ruptura (tb), la cantidad de colorante removida por gramo de Q al tiempo de ruptura (qb) y a las 70 horas (q70).
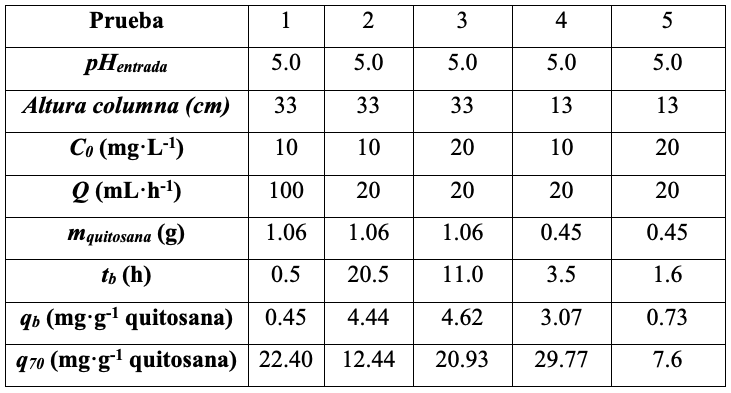
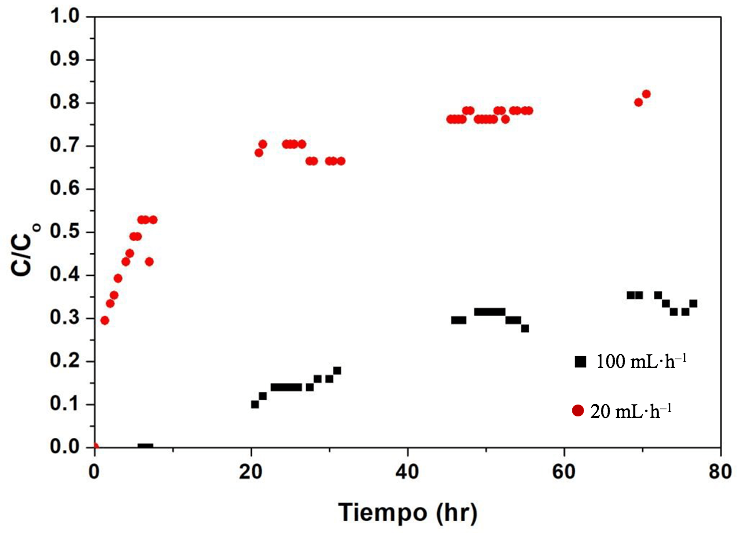
Efecto de la velocidad de flujo. Se empacó la columna de 33 cm con 42,3 g de hidrogel de Alg-Q (1,06 g Q) y se hizo fluir una disolución de colorante a una concentración de 10 mg·L–1 y pH igual a 5,0. Las velocidades de flujo utilizadas fueron 20 y 100 mL·h–1. Las pruebas 1 y 2 de la Tabla 1 muestran que el tiempo de ruptura es mucho menor al aumentar el flujo y que la cantidad de colorante adsorbida en el punto de ruptura es aproximadamente 10 veces menor cuando la velocidad de flujo se quintuplica. Esto se debe a que al aumentar la velocidad de flujo una mayor cantidad de colorante se pasa por unidad de tiempo, de manera que el adsorbente y el colorante tienen una menor oportunidad de interaccionar entre sí [10].
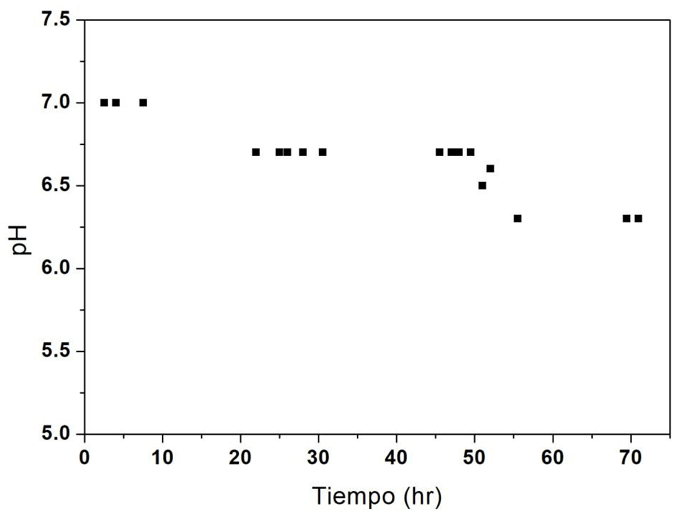
En la Figura 3 se muestran las curvas de avance obtenidas. En ellas se observa que después de que se alcanzara el punto de ruptura, la concentración del efluente a la salida de la columna se incrementó rápidamente, pero posteriormente aumentó lentamente y al final del experimento (70 horas) la columna todavía no se saturaba. La saturación de la columna ocurre de manera muy lenta, lo cual se atribuye a que el colorante tiene que difundirse a través del hidrogel para llegar al adsorbente (Q). Un acercamiento lento a la saturación ha sido previamente reportado como una característica común de procesos de adsorción donde la difusión es el proceso limitante de transferencia de masa [16,17]. Otro factor que puede explicar que las columnas no se saturen durante los experimentos es que las soluciones de colorante a la salida de las columnas tenían un pH cercano a 7,0, pH mayor que el de entrada, por lo que se generan nuevos grupos amino cargados positivamente que pueden adsorber más colorante. El pH a la salida disminuía un poco al pasar más solución por la columna (Figura 4). En todos los experimentos se presentó el fenómeno de que el pH se incrementaba a la salida de la columna.
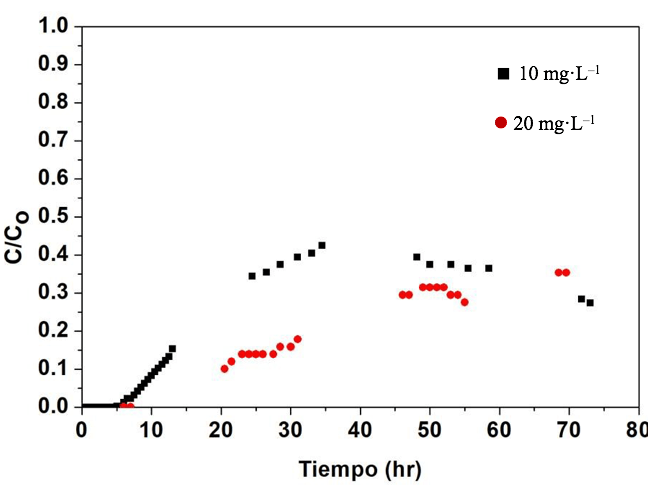
Efecto de la concentración inicial de colorante. Para estudiar el efecto de la concentración de colorante se utilizaron columnas de 33 cm de altura empacadas con 42,3 g de hidrogel de Alg-Q (1,06 g Q) y de 13 cm de altura empacadas con 17,7 g de hidrogel de Alg-Q (0.45 g Q) y se hizo pasar una disolución acuosa de Rojo 40 a pH de 5,0 a un flujo de 20 mL·h–1. Las concentraciones iniciales estudiadas fueron 10 y 20 mg·L–1. En la Tabla 1 al comparar la prueba 2 con la 3 y la 4 con la 5 se observa que al duplicar la concentración inicial de colorante, el punto de ruptura se alcanzó casi a la mitad del tiempo, lo cual se debe a que un mayor gradiente de concentración causó una mayor velocidad de transferencia de masa [18]. Al comparar los valores de qb reportados en la Tabla 1 entre las pruebas 2 y 3, y las pruebas 4 y 5, se observa que la capacidad de adsorción fue mayor en el punto de ruptura al aumentar la concentración inicial de colorante, lo cual se atribuye a la mayor transferencia de masa ocasionada por un mayor gradiente de concentración.
La Figura 5 muestra las curvas de avance cuando se utilizó la columna de 33 cm utilizando un flujo de la solución de colorante de 20 mL·h–1, un pH 5,0 y dos concentraciones (10 y 20 mg·L–1), en ella se observa que después de que se alcanzara el punto de ruptura, la concentración del efluente a la salida de la columna se incrementó rápido, pero posteriormente aumentó lentamente y al final del experimento (70 horas) la columna no se saturaba; similar resultado se obtuvo cuando se utilizó la columna de 13 cm. Como se explicó anteriormente, el que no se saturará la columna se puede deber a limitación de transferencia de masa y a la formación de nuevos centros activos por la transferencia de protones de la solución al adsorbente.
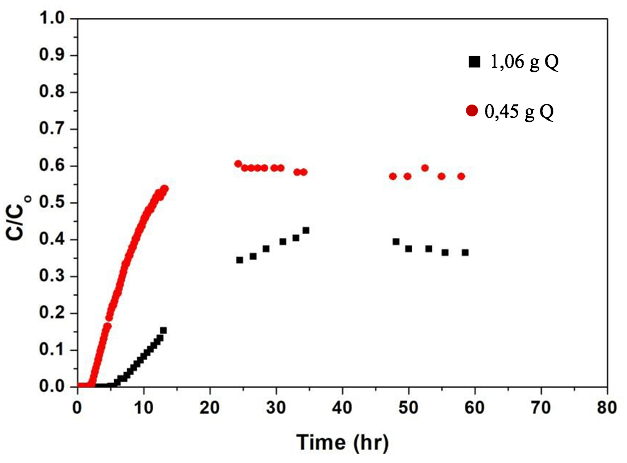
Efecto de la altura de la columna. El efecto de la altura de la columna (cantidad de adsorbente) se determinó utilizando dos columnas empacadas con Alg-Q de diferentes alturas: 33 y 13 cm (1,06 y 0,45 g de Q, respectivamente). Las columnas fueron alimentadas con disoluciones de Rojo 40 de 10 y 20 mg·L–1 con un pH de 5.0, a una velocidad de flujo de 20 mL·h–1. Se compararon el experimento 2 con el 4 y el experimento 3 con el 5 (Tabla 1). Al aumentar el tamaño de la columna (mayor cantidad de adsorbente) aumenta la capacidad de adsorción en el punto de ruptura, lo cual se atribuye a un mayor número de sitios de adsorción disponibles para interactuar con el colorante y a un mayor tiempo de contacto entre el colorante y el adsorbente [19,20]. El incremento en la altura del lecho crea una mayor distancia a recorrer para que la zona de transferencia de masa alcance la salida de la columna, subsecuentemente, resultando en mayor tiempo de ruptura [21].
La Figura 6 muestra las curvas de avance cuando se utilizó un flujo de 20 mL·h1, un pH de 5,0 y las columnas de 33 y 13 cm; después de que se alcanzara el punto de ruptura, la concentración del efluente a la salida de las columnas se incrementó rápido pero luego aumentó lentamente y al final del experimento (70) la columna todavía no se saturaba. Similares resultados se obtuvieron cuando se utilizó un flujo de 10 mL·h1.
CONCLUSIONES
Se obtuvieron hidrogeles de alginato–quitosano donde la concentración del adsorbente (Q) en los hidrogeles fue 2,5%. Estos hidrogeles fueron utilizados para empacar columnas de percolación para remover colorante Rojo 40 de disoluciones acuosas.
Se encontró que al aumentar la velocidad de flujo, se alcanzó el tiempo de ruptura más pronto. Al aumentar la concentración inicial del Rojo 40, se obtuvo mayor capacidad de adsorción, lo cual se debe a una mayor transferencia de masa al existir un mayor gradiente de concentración. Al aumentar la altura de la columna (mayor cantidad de adsorbente) la capacidad de adsorción del colorante aumentó debido al mayor número el número de sitios disponibles para interactuar con el colorante previo a la salida de la disolución de la columna.
El lento acercamiento a la saturación de las columna es un comportamiento que difiere del que típicamente se observa en las columnas de adsorción y se explica por limitaciones en la transferencia de masa del colorante debido a que el adsorbente se encuentra disperso en el hidrogel y a la formación de nuevos grupos por la continua protonación de grupos amino del Q, lo cual genera nuevos sitios capaces de adsorber colorante.
Agradecimientos. Esta investigación fue realizada con el apoyo económico otorgado por el CONACYT (CB–2014–1–241108). Tres de los autores (I.P.V.N., D.A.V., S.I.Y.B.) agradecen la beca otorgada por el CONACYT.
BIBLIOGRAFÍA
[1] Piccin, J. S., Dotto, G. L., Vieira, M. L., & Pinto, L. A. (2011). Kinetics and mechanism of the food dye FD&C Red 40 adsorption onto chitosan. Journal of Chemical & Engineering Data, 56(10), 3759-3765.
[2] Chougui, A., Zaiter, K., Belouatek, A., & Asli, B. (2014). Heavy metals and color retention by a synthesized inorganic membrane. Arabian Journal of Chemistry, 7(5), 817-822.Chicago
[3] El-Ashtoukhy, E. S., & Fouad, Y. O. (2015). Liquid–liquid extraction of methylene blue dye from aqueous solutions using sodium dodecylbenzenesulfonate as an extractant. Alexandria Engineering Journal, 54(1), 77-81.
[4] Tchamango, S. R., Kamdoum, O., Donfack, D., & Babale, D. (2017). Comparison of electrocoagulation and chemical coagulation processes in the treatment of an effluent of a textile factory. Journal of Applied Sciences and Environmental Management, 21(7), 1317-1322.
[5] Zhou, T., Lu, W., Liu, L., Zhu, H., Jiao, Y., Zhang, S., & Han, R. (2015). Effective adsorption of light green anionic dye from solution by CPB modified peanut in column mode. Journal of Molecular Liquids, 211, 909-914.
[6] Ahmad, M., Manzoor, K., & Ikram, S. (2017). Versatile nature of hetero-chitosan based derivatives as biodegradable adsorbent for heavy metal ions; a review. International journal of biological macromolecules, 105, 190-203.
[7] Crini, G., & Badot, P. M. (2008). Application of chitosan, a natural aminopolysaccharide, for dye removal from aqueous solutions by adsorption processes using batch studies: a review of recent literature. Progress in polymer science, 33(4), 399-447.
[8] Zhang, J., Zhou, Q., & Ou, L. (2011). Kinetic, isotherm, and thermodynamic studies of the adsorption of methyl orange from aqueous solution by chitosan/alumina composite. Journal of Chemical & Engineering Data, 57(2), 412-419.
[9] Bhatnagar, A., & Sillanpää, M. (2009). Applications of chitin-and chitosan-derivatives for the detoxification of water and wastewater—a short review. Advances in colloid and Interface science, 152(1-2), 26-38.
[10] López-Cervantes, J., Sánchez-Machado, D. I., Sánchez-Duarte, R. G., & Correa-Murrieta, M. A. (2018). Study of a fixed-bed column in the adsorption of an azo dye from an aqueous medium using a chitosan–glutaraldehyde biosorbent. Adsorption Science & Technology, 36(1-2), 215-232.
[11] Rouf, S., & Nagapadma, M. (2015). Modeling of fixed-bed column studies for adsorption of azo dye on chitosan impregnated with a cationic surfactant. International Journal of Scientific and Engineering Research, 6(2), 124-132.
[12] Vieira, M. L. G., Esquerdo, V. M., Nobre, L. R., Dotto, G. L., & Pinto, L. A. A. (2014). Glass beads coated with chitosan for the food azo dyes adsorption in a fixed bed column. Journal of Industrial and Engineering Chemistry, 20(5), 3387-3393.
[13] Gotoh, T., Matsushima, K., & Kikuchi, K. I. (2004). Preparation of alginate–chitosan hybrid gel beads and adsorption of divalent metal ions. Chemosphere, 55(1), 135-140.
[14] Jeon, Y. S., Lei, J., & Kim, J. H. (2008). Dye adsorption characteristics of alginate/polyaspartate hydrogels. Journal of Industrial and Engineering Chemistry, 14(6), 726-731.
[15] Verduzco–Navarro, I.P., Ríos–Donato, N., Mendizabal, E., Katime, I. (2016). Remoción de colorante Rojo 40 mediante de perlas de alginato–quitosano y alginato– sulfato de quitosano. Revista de Ciencias Ambientales y Recursos Naturales, 2(3), 33-43.
[16] Aksu, Z., & Gönen, F. (2006). Binary biosorption of phenol and chromium (VI) onto immobilized activated sludge in a packed bed: prediction of kinetic parameters and breakthrough curves. Separation and Purification Technology, 49(3), 205-216.
[17] Tovar-Gómez, R., Moreno-Virgen, M. R., Dena-Aguilar, J. A., Hernández-Montoya, V., Bonilla-Petriciolet, A., & Montes-Morán, M. A. (2013). Modeling of fixed-bed adsorption of fluoride on bone char using a hybrid neural network approach. Chemical engineering journal, 228, 1098-1109.
[18] Aksu, Z., Çağatay, Ş. Ş., & Gönen, F. (2007). Continuous fixed bed biosorption of reactive dyes by dried Rhizopus arrhizus: Determination of column capacity. Journal of hazardous materials, 143(1-2), 362-371.
[19] Liu, D., & Sun, D. (2012). Modeling adsorption of Cu (II) using polyaniline-coated sawdust in a fixed-bed column. Environmental Engineering Science, 29(6), 461-465.
[20] Sadaf, S., & Bhatti, H. N. (2014). Batch and fixed bed column studies for the removal of Indosol Yellow BG dye by peanut husk. Journal of the Taiwan Institute of Chemical Engineers, 45(2), 541-553.
[21] Saad, D. M., Cukrowska, E., & Tutu, H. (2015). Column adsorption studies for the removal of U by phosphonated cross-linked polyethylenimine: modelling and optimization. Applied Water Science, 5(1), 57-63.
