Nino Castro Mandujano1, Jenny Álvarez Bautista2, Oscar Tinoco Gómez3, José Luis López1
1Departamento de Química Orgánica, Facultad de Química e Ingeniería Química, UNMSM. Av. Germán Amezaga 375, Cercado de Lima, Lima, Perú. Correo electrónico: ocastrom@unmsm.edu.pe
2Departamento de Química Analítica, Facultad de Química e Ingeniería Química, UNMSM, Av. Germán Amezaga 375, Cercado de Lima, Lima, Perú. Correo electrónico: jenny.alvarez73@yahoo.com
3Facultad de Ingeniería Industrial, Universidad Nacional Mayor de San Marcos–UNMSM. Av. Germán Amezaga 375, Cercado de Lima, Perú. Correo electrónico: otinocog@gmail.com
Recibido: Noviembre 2019; Aceptado: Febrero 2020
Texto completo (pdf)
Cita (APA)
Castro Mandujano, N., Álvarez Bautista, J., Tinoco Gómez, O., López, J. L., (2020). Recuperación de proteínas del efluente “agua de cola” de la industria de harina de pescado con quitosano calcáreo. Revista Iberoamericana de Polímeros, 21(2), 41-50.
RESUMEN
La investigación aborda el saneamiento de efluentes de la industria de harina de pescado específicamente los residuos acuoso llamado “agua de cola”, cuyos contaminantes son las proteínas, grasas, sales, etc.; utilizando el biopolímero quitosano calcáreo Q1, obtenido a nivel piloto, a partir de las cabezas del langostino rojo (Litopanaeus vannamei) que también es un residuo orgánico de las industrias langostineras del norte del Perú. Para obtener el quitosano calcáreo Q1, se aplicó la desproteinización y la desacetilación con NaOH, a 10 y 50%, respectivamente; para optimizar se analizó los parámetros de concentración, tiempo, relación masa/solución de NaOH, etc. Para la floculación del residuo acuoso “agua de cola”, se analizó los parámetros como el pH de la solución, volumen de floculante, etc. Se obtuvo quitosano calcáreo de 11,9 de humedad, 2,55 de cenizas, 7,77 de nitrógeno, 89,32 de grado de desacetilación, con 731 cP de viscosidad y 925 kDa de peso molecular. Se obtuvieron porcentajes muy significativos sobre la floculación del residuo acuoso, el cual se logró flocular a un pH de 5,5 con quitosano 0,015%; luego, se filtró y se recuperó un sólido proteico–grasas–sales (5,33g de sólido proteína y grasa por 100 mL de residuo acuoso “agua de cola”) que se puede emplear como producto balanceado para alimento de aves y peces, además, se obtuvo un líquido ligeramente amarillo cuya características fisicoquímicas son: 0,11 de sólidos totales, 0,08 de proteína, 0,01 de grasa, 0,02 de cenizas, y 0,02% de NNP.
ABSTRACT
The research addresses the sanitation of effluents from the fishmeal industry specifically the aqueous waste called “cola water”, whose contaminants are proteins, fats, salts, etc, using the CHCa limestone chitosan biopolymer, obtained at a pilot level, from the heads of the red shrimp (Litopanaeus vannamei) which is also an organic residue of the shrimp industries of northern Peru. To obtain the calcareous chitosan, deproteinization and deacetylation with NaOH were applied, at 10 and 50% respectively; to optimize the parameters of concentration, time, mass / solution ratio of NaOH, etc. were analyzed. For the flocculation of the “tail water” aqueous residue, the parameters such as solution pH, flocculant volume, etc. were analyzed. Calcareous chitosan of 11.9 moisture, 2.55 ash, 7.77 nitrogen, 89.32 deacetylation degree was obtained, with 731 cP viscosity and 925 kDa molar mass. Very significant percentages were obtained on the flocculation of the aqueous residue, which was flocculated at a pH of 5.5 with 0.015% chitosan; then, a protein–fat–salt solid (5.33 g of solid of protein and fat per 100 mL of residue) was filtered and can be used as a balanced product for poultry and fish feed, in addition, a slightly yellow liquid was obtained whose characteristics physicochemicals are: 0.11 total solids, 0.08 protein, 0.01 fat, 0.02 ash, and 0.02% NNP.
INTRODUCCIÓN
Un problema ambiental en el norte del Perú son los residuos orgánicos de las industrias langostineras, tras la extracción de la parte comestible; estos residuos (caparazones y cabezas de los langostinos) albergan un polímero natural llamado quitina; pero, de esta biomasa, el menos utilizado son las cabezas, a partir del cual, también se puede obtener quitina y el quitosano.
El quitosano es un polisacárido catiónico lineal, que se obtiene por desacetilación de la quitina. Las propiedades del quitosano justifican la aplicabilidad de este biopolímero en diversos campos [1]. Los grupos aminos e hidroxilos presentes en su estructura, le confieren la capacidad de derivatización, obteniéndose una variedad de sustancias con propiedades específicas y valiosas en sus respectivos campos de aplicación. Las diversas aplicaciones son: biomédicas, farmacéuticas, en alimentos, en agricultura, en tratamiento de aguas, en cosmética, etc. [2].
Los problemas ambientales en ecosistemas marinos han sido causados principalmente por la actividad de las pesquerías. Una de las consecuencias de la instalación de plantas industriales de harina de pescado, ha sido la contaminación, debido a la descarga de sus desechos (agua de cola, agua de bombeo y desechos del corte principalmente) sobre las aguas marinas. El entorno de la industria se convierte en un ecosistema particular, por la adición de residuos orgánicos, como lo son escamas, sanguaza, agua de cola, combustible y grasas, que generan la formación de sedimentos negruzcos con olores sulfurosos, lo cual genera alteraciones en el sedimento y en el agua de mar, causando un desequilibrio en las propiedades físicas, químicas y biológicas. El agua de cola está compuesta principalmente de proteínas y grasas [3].
En la Figura 1 tenemos el diagrama de flujo de la fabricación de harina de pescado, en la cual se observa las salidas del agua de bombeo y agua de cola. Después que llegan los barcos a orillas de la playa, los peces son llevados a la planta de harina de pescado, luego pasan a los procesos de cocción y prensado, los sólidos continúan el proceso de harina y la fracción líquida mediante centrifugación se separa los aceites del agua de cola. Para el tratamiento de este residuos acuoso que contiene material orgánico que pueden ser proteínas y grasas principalmente; existen varios métodos como el biotratamiento con el cultivo de algas y bacterias (pseudomonas y actinomicetos, etc.), este método funciona bien pero solo a nivel pequeño, cuando se quiere emplear a nivel industrial se complica manejar los parámetros, por otro lado, además de obtener el agua tratada limpio, también se obtiene microalgas que debe eliminarse subsecuentemente y además gran parte del fósforo permanece en el agua después del tratamiento. También, hay otro método que es por desinfección con cloro, es decir la cloración, si es un buen método para grandes cantidades, bajo costo, pero; el cloro va al ambiente, esto implica contaminación del aire o capa de ozono, además hay reacciones secundarias con el amoniaco como la formación de monocloroaminas, di o tricloroaminas, estos son cancerígenos. Otro método interesante es la microburbuja, es un sistema de flotación por aire inducido, así tenemos a las proteínas flotando debido a las adherencias de las microburbujas pero se complica al aplicarlo a nivel industrial [4].
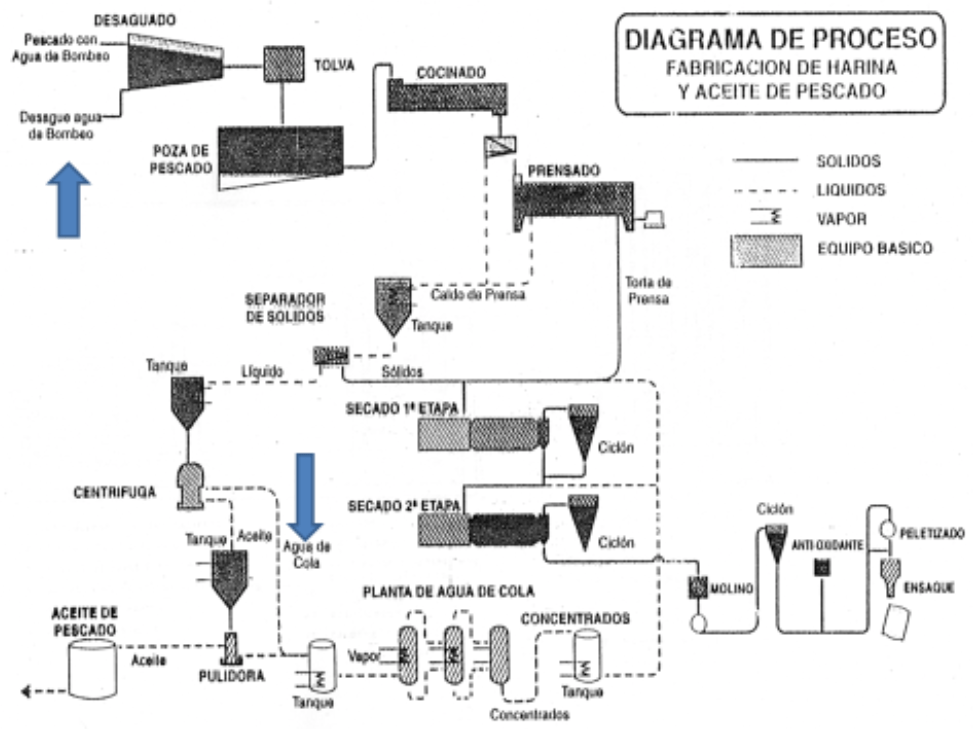
En este sentido el objetivo de la presente investigación es recuperar las proteínas y grasas del residuo acuoso (agua de cola) de las industrias de harina de pescado con un biopolímero (quitosano calcáreo) mediante el proceso de floculación.
PARTE EXPERIMENTAL
La muestra. Los residuos de cabezas de langostino (Litopanaeus vannamei) fue proporcionada por la empresa Congelados Pacifico S.A. y el residuo acuoso “agua de cola” fue proporcionada por la empresa “TASA”.
Obtención del quitosano calcáreo. Para obtener el quitosano calcáreo a partir de las cabezas de los langostinos (Litopanaeus vannamei), se realizaron las siguientes etapas [2, 5]:
Proceso de desproteinización (DP). Las cabezas así húmedas, fueron tratados con soluciones de NaOH 8%; la temperatura de las pruebas la temperatura generada por la disolución “in situ”, por 90 minutos (condiciones óptimas según [5, 6]). Después, la solución fue filtrada y el material sólido se lavó con agua sucesivamente hasta alcanzar pH neutro. Todas las soluciones básicas se guardan.
Proceso de desacetilación (DA). El producto obtenido en la etapa anterior, después de realizar la DP se llama quitina calcárea, luego, a esta muestra húmeda se realizó el proceso llamado desacetilación el cual consistió en tratar con soluciones de NaOH 50%, el tiempo de reacción fue de 2 horas, la temperatura se mantuvo de 95–100°C. Después, la solución fue filtrada y el material sólido se lavó con agua sucesivamente hasta alcanzar pH neutro, obteniéndose quitosano de color blanco Q1. La solución básica se ha guardado para otros procesos. Luego, el sólido blanco, es decir, el quitosano calcáreo húmedo, fue secado en una estufa a 40°C durante 3 días, después se procedió a molerlo a un malla de 20 [6, 7]. Adicionalmente se repitió el proceso de desacetilación explicado anteriormente, un nuevo proceso adicional por dos horas se obtuvo el quitosano Q2, a parte, se realizó un nuevo proceso de desacetilación por un periodo de 4 horas, así se obtuvo el quitosano Q3.
Caracterización de quitina y quitosano. En esta parte se realizaron varios análisis que ya se ha explicado en un artículo publicado por Álvarez [7] y para los detalles teóricos se revisó la referencia [2] los siguientes análisis:
a. Determinación de Nitrógeno. La determinación del contenido de nitrógeno se realizó por el Método Kjeldahl [8].
b. Determinación del porcentaje de humedad. Se determina normalmente por gravimetría; para ello, se lleva a peso constante una muestra calentada en una estufa a 105ºC, durante 4 horas [9].
c. Determinación de cenizas.– según la referencia [9].
d. Determinación del grado de desacetilación. Este parámetro se determinó mediante espectroscopia IR [7, 10]; también se utilizó espectroscopia UV – primera derivada; este método aplicado fue propuesto en 1985 por Muzzarelli y Rochetti [11] y hace uso de la primera derivada de los espectros UV de la N–acetil–D–glucosamina (NAG), del quitosano y de disoluciones de ácido acético.
e. Determinación del peso molecular. Con el método viscosimétrico de Ostwald se determinó la viscosidad del quitosano, y aplicando la ecuación de Mark–Houwink-Sakurada de calculó el peso molecular [2, 13].
Caracterización del efluente. Se caracteriza el efluente “agua de cola” antes y después del tratamiento, teniendo en cuenta las referencias para los análisis respectivos [8, 14], para ello se ha realizado los siguientes análisis:
- Análisis de sólidos totales
- Análisis de sólidos disueltos
- Determinación de porcentaje de nitrógeno no proteico NNP
- Determinación de proteínas totales
- Determinación de pH
- Determinación de grasas
Proceso de floculación con quitosano calcáreo. Para este proceso se ha considerado los siguientes parámetros:
- pH de la solución.
- Concentración de la solución de quitosano.
- Volúmen de quitosano.
Para cada proceso se ha mantenido constante algunas variables, como el volumen del residuo acuoso (200 mL), la velocidad de agitación de 120 rpm, pH inicial del residuo 6,20–6,40 y el tiempo de floculación que es el periodo de 30 minutos.
El proceso consiste en colocar 200 mL de solución básica proteica (agua de cola), se realizan varias pruebas con las siguientes variaciones:
- Concentración de la solución de quitosano: 0,100, 0,050, 0,025, 0,020, 0,015, 0,010, y 0,005
- Volumen de la solución de quitosano 5, 10, 15, 20, y 25 mL
- Grado de desacetilación de quitosano: 99, 96, y 89%,
- pH de la solución antes de flocular 5,0; 5,5; 6,0 y 6,5.
Después, de esperar 30 minutos, se filtra y se analiza tanto el líquido filtrado como el sólido obtenido.
RESULTADOS
La caracterización de la muestra (cabezas del langostinos Litopanaeus vannamei) fue determinando su porcentaje de humedad, cenizas, nitrógeno, quitina, quitosano y quitosano calcáreo obtenido; estos resultados se muestran en la Tabla 1. Además, en esta tabla se observa los porcentajes de quitina, quitosano y quitosano calcáreo obtenidos, esto significa los rendimientos de quitina y quitosano, ver Tabla 1.
El proceso de obtención de quitosano calcáreo se realizó en un reactor, el cual es un tanque cilíndrico de acero inoxidable de 75 L de capacidad que cuenta con un sistema electrónico de control de temperatura, paletas de agitación y selector de velocidad. La muestra, cabezas de langostino, se trabajó tal como la empresa langostinera lo desecha, donde su humedad es alta, alrededor de 52%, además contiene carotenos, proteínas, grasas, etc. La metodología realizada para la desproteinización y desacetilación es según Castro [2, 6].

Todo el proceso de obtención del quitosano calcáreo son ecológicos y ecoeficientes ya que no generan residuos. Los residuos acuosos (soluciones acuosas ácidas y básicas, tanto de los filtrados y los lavados) se pueden reutilizar y/o reciclar.
La caracterización del biopolímero (quitosano calcáreo) se realizó determinando su porcentaje de humedad, cenizas, nitrógeno, desacetilación, viscosidad y masa molar según las referencias [2, 6], todos estos resultados están en forma resumida en la Tabla 2.
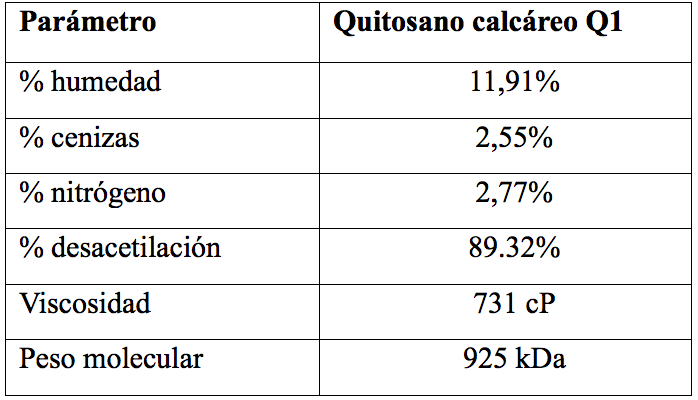
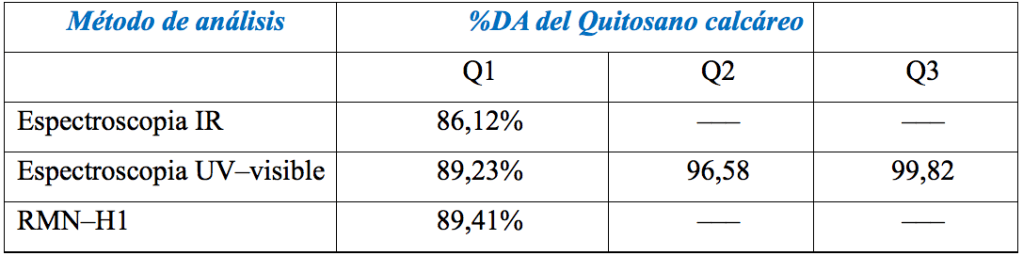
Para el caso de la determinación del porcentaje del DA hay 3 métodos los cuales han sido explicados ampliamente en otras publicaciones de los autores [2, 6]. Pero, cabe resaltar que al comparar estos 3 métodos, para el quitosano Q1, los métodos con mayor exactitud y precisión son el espectrofotómetro UV–Visible y la RMN–H1; mientras que el método espectrofotométrico IR, no es muy exacto, a pesar que se hicieron 5 repeticiones, en la Tabla 3, vemos la comparación de estos valores. Por otro lado, para los otros tipos de quitosano Q2 y Q3 solo se determinaron el grado de desacetilación %DA, por el método de espectroscópico UV–visible.
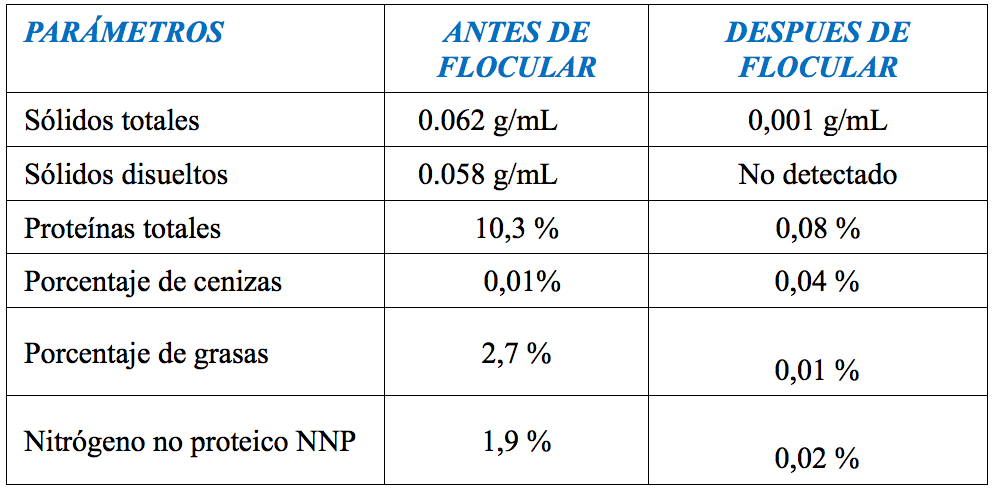
La muestra de agua de cola, es de color crema, tal como se observaba en la Figura 2, el cual fue proporcionado por la empresa TASA, del Callao – Perú. A esta muestra se realizó un análisis de algunos parámetros fisicoquímicos, estos resultados lo vemos en la Tabla 4, otro dato importante es que el pH inicial de este efluente es pH 6,20–6,40, el cual puede ir variando ligeramente por el tema de la descomposición, en fresco el agua de cola, tiene el pH 6,37.

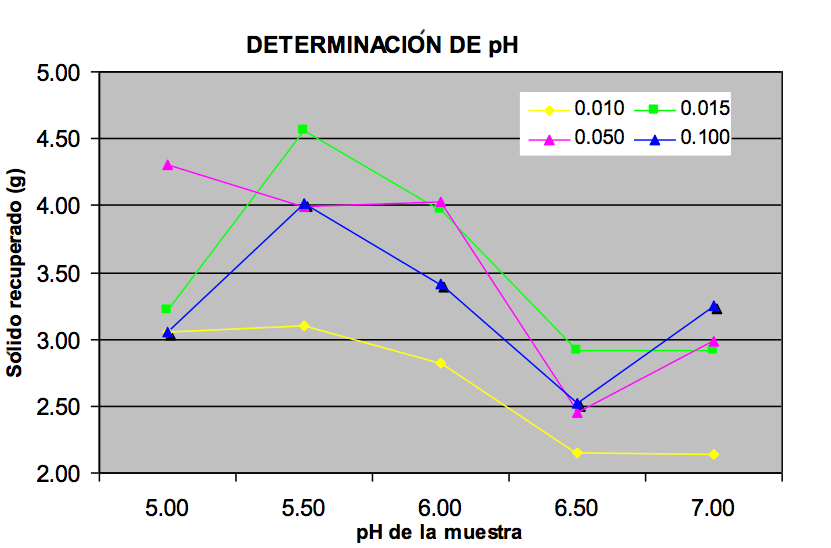
En la Figura 3, tenemos la gráfica de sólido recuperados en función del pH, para diferentes concentraciones, analizando la gráfica observamos que hay un máximo de sólidos recuperados a pH = 5,50, y todo esto a una concentración de 0,015% de quitosano, así determinamos dos parámetros de optimización del proceso de floculación del material orgánico (proteínas, grasas, sales, carotenos, etc.), este pH, nos dio 4,5558 gramos de sólido recuperados a partir de 200 mL de efluente. Además, se ha observado que el vaso a pH 5,5 mejor ha floculado a la concentración de quitosano Q1 de 0,015%.
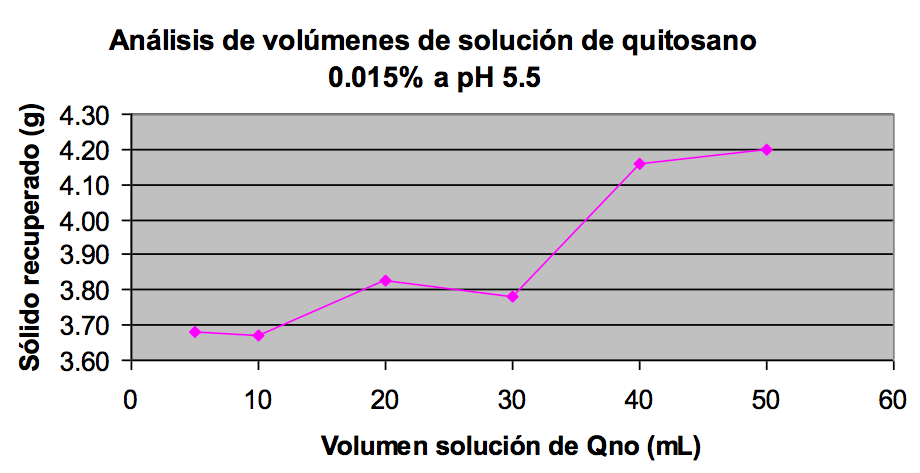
En la Figura 4, en base a los pesos de los sólidos recuperados confirma que a la concentración de 0,015% y a pH 5,5 se observa un máximo peso de recuperación, esto ocurre a volumen de 40 mL de esta solución de quitosano diluido.
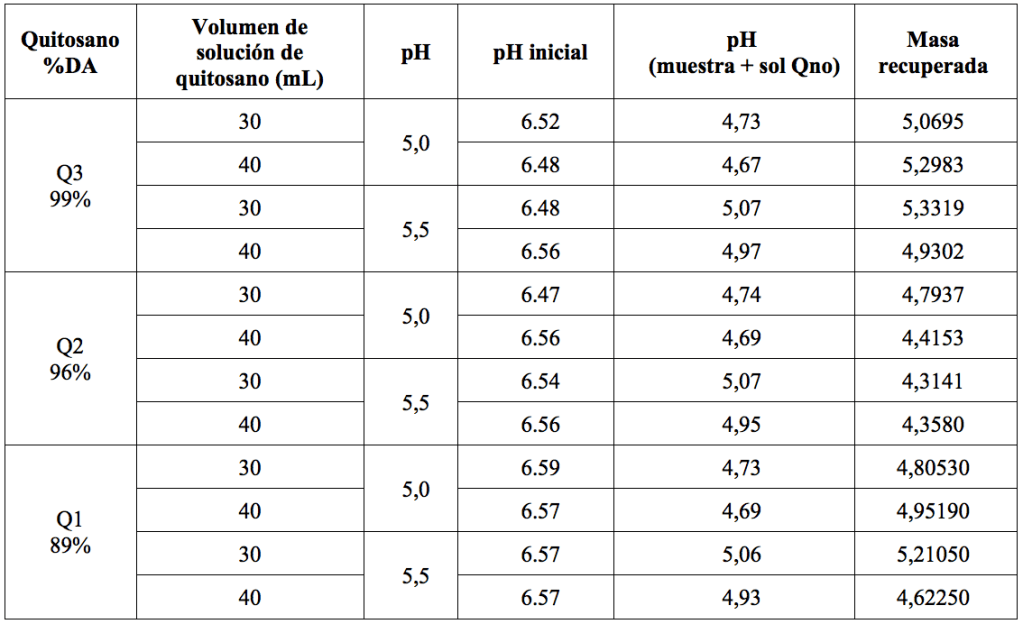
En la Tabla 5, se observa el análisis de floculación variando el grado de desacetilación %DA del quitosano calcáreo a partir de las cabezas; se deduce que al ser mayor el grado de desacetilación sus grupos aminos NH2, aumentan es decir se hace más polar, más soluble en medio ácido y se extiende con mayor facilidad, permitiendo así, atrapar a los flósculos de las proteínas y grasas para luego precipitar. En nuestro caso se observa que a pH 5,5 hay mayor recuperación de sólidos proteicos 5,3319 gramos. Entonces, podemos afirmar, que las condiciones óptimas del proceso de recuperación de proteínas y grasas son: pH entre 5,5 y 5, de concentración de quitosano: 0.015%; con relación floculante–efluente: de 30/200 y 40/200. Además, el quitosano de bajo grado de desacetilación presenta menor polaridad, disminuye su capacidad de neutralizar cargas de los coloides en suspensión. Mientras que el quitosano con alto grado de desacetilación provenientes de cabezas de langostino experimentan las mejores recuperaciones de proteínas del efluente, que contiene 5,33 gramos de sólidos totales recuperados del residuo acuoso “agua de cola” y de esto 5,04 gramos fue proteínas.
CONCLUSIONES
Se obtuvo quitosano calcáreo (Q1) de las cabezas de langostino, a nivel piloto con las siguientes características: 11,9 de humedad, 2,55 de cenizas, 7,77 de nitrógeno, 89,32 de grado de desacetilación y 925 kDa de peso molecular. Además realizando otros proceso adicionales de desacetilación se obtuvo quitosano con desacetilación de 96 (Q2) y 99% (Q3). Se logró flocular al efluente llamado “agua de cola” de una industria de harina de pescado a un pH de 5,5 con quitosano calcáreo 0,015%. Se obtuvo un sólido proteico–grasas–sales (3,86 g de sólido por 100 mL de residuo). Las características fisicoquímicas del efluente después de tratar con quitosano calcáreo Q1, son: 0,11 de sólidos totales, 0,08 de proteína, 0,0 de grasa, 0,02 de cenizas, y 0,02 de NNP.
Agradecimientos. Se agradece a la Empresa de harina de pescado TASA, por la donación de la muestra de “agua de cola”. También agradecemos a la empresa Congelados Pacífico S.A. la cesión de las cabezas de langostinos.
BIBLIOGRAFÍA
[1] Castro O ”Química del quitosano y sus aplicaciones”. Editorial académica Española, España. (2017)
[2] Pastor A “Quitina y quitosano: obtención, caracterización y aplicaciones”. CYTED, Lima, Fondo Editorial de la Pontificia Universidad Católica del Perú. (2004).
[3] Cabrera C, Rev. Instituto de Investigación (RIIGEO), FIGMMG–UNMSM, 2(3) (1999)
[4] Garcia C, Pacheco R, Valdez S, J. Food, 7(1), 67, DOI: 10.1080/11358120902850412
[5] Valerio M, Campana S, Quim. Nova, 31(8), 2014 (2008)
[6] Chávez A, Colina M, Valbuena A, López A, Rev. Iberoamericana de Polímeros, 13(2), 41 (2012)
[7] Álvarez J, Castro O, Tinoco O, Rev. Iberoamericana de Polímeros, 20(3), 90 (2019)
[8] A.S.T.M, Designation E 258 – 67 (Reapproved 1987).
[9] AOAC, Official methods of analysis of the Association of Official Analytical Chemists, 15th ed., 1990.
[10] Brugnerotto J, Lizardi J, Goycoolea F, Argüelles W, Desbrieres J, Rinaudo M, Polymer, 42, 3569 (2001)
[11] Muzarelli R, Rochetti R, Carbohydrate Polymer, 5, 461 (1985)
[12] Lavertu M, Xia A, Serreqi A, Berrada M, Rodrigues A, Wang D, Bushman M, Gupta A, J. Pharm. Biom. Research, 32, 1149 (2003)
[13] Dos Santos JE, Soares J, Dockal ER, Campana SP, Cavalheiro ET, Polímeros: Ciencia e Tecnología, 13(4), 242 (2003)
[14] Hans R “Laboratory manual for the examination of water, waste water and soil”, 2ª edición, Ed. Weinheim VCH, 1992
