Jenny Álvarez B.1, O. Nino Castro M.2*, Oscar Tinoco G.3
1 Departamento de Química Analítica, Facultad de Química e Ingeniería Química, UNMSM. Av. Germán Amezaga 375, Cercado de Lima, Lima, Perú
2 Departamento de Química Orgánica, Facultad de Química e Ingeniería Química, UNMSM, Av. Germán Amezaga 375, Cercado de Lima, Lima, Perú. Correo electrónico: ocastrom@unmsm.edu.pe
3 Facultad de Ingeniería Industrial, Universidad Nacional Mayor de San Marcos–UNMSM. Av. Germán Amezaga 375, Cercado de Lima, Perú
Recibido: Febrero 2019; Aceptado:Abril 2019
Texto completo (pdf)
Cita (APA)
Álvarez B., Jenny, Castro M., O. Nino, Tinoco G., Oscar (2019). Adsorción de azul de metileno con biopolímeros (quitosano calcáreo y quitosano) obtenidos de las cabezas de langostinos a nivel piloto. Revista Iberoamericana de Polímeros, 20(3), 90-104.
RESUMEN
La investigación aborda el saneamiento de efluentes textiles contaminados por colorantes, utilizando biopolímeros (quitosano Ch y quitosano calcáreo ChCa) obtenidos a partir de las cabezas del langostino rojo (Litopanaeus vannamei) para la adsorción del azul de metileno, con la evaluación de parámetros como el pH de la solución, concentración inicial del colorante, tamaño de adsorbente, etc. Se obtiene quitosano a partir de las cabezas de langostino en tres etapas: desproteinización, desmineralización y desacetilación y, para quitosano calcáreo sólo se desproteiniza y desacetila. Ambos biopolímeros se caracterizan determinando su grado de desacetilación (por ultravioleta–visible y resonancia magnética nuclear–H), peso molecular, viscosidad y otras propiedades fisicoquímicas. Se obtuvieron porcentajes significativos de adsorción del colorante (azul de metileno de 200 ppm); el quitosano Ch 1020, en 30 minutos, fue adsorbido el 77% a un pH óptimo de 7,5; el quitosano calcáreo ChCa 1020 tuvo adsorción del 81% a los 35 minutos, a pH 8,0.
ABSTRACT
The research deals with the sanitation of textile effluents contaminated by dyes, using biopolymers (chitosan Ch and chitosan calcareous CHCa) obtained from the heads of the red shrimp (Litopanaeus van-namei) for the adsorption of methylene blue, with the evaluation of parameters such as pH of the solution, initial concentration of the dye, size of adsorbent, etc. Chitosan is obtained from the heads of shrimp in 3 stages: deproteinization, demineralization and deacetylation; and, for calcareous chitosan it is only deproteinized and deacetylated. Both biopolymers are characterized by determining their degree of deacetylation (by ultraviolet–visible and nuclear magnetic resonance–H), molar weight, viscosity and other physico-chemical properties. Significant percentages of dye adsorption were obtained (methylene blue 200 ppm); the chitosan Ch1020, in 30 minutes, was adsorbed 77% at an optimum pH of 7.5; ChCa 1020 calcareous chitosan had 81% adsorption at 35 minutes at pH 8.0.
INTRODUCCIÓN
Un problema ambiental en el norte del Perú son los residuos de las industrias langostineras, tras la extracción de la parte comestible; estos residuos (caparazones y cabezas de los langostinos) albergan un polímero natural llamado quitina; pero, de esta biomasa, lo menos utilizado son las cabezas, a partir de la cuál, también se puede obtener quitina y quitosano.
La quitina es un polisacárido compuesto de unidades de N–acetil–D–glucos–2–amina. Éstas están unidas entre sí con enlaces β–1,4, de la misma forma que las unidades de glucosa componen la celulosa. Esto permite un incremento de los enlaces de hidrogeno con los polímeros adyacentes, dándole al material una mayor resistencia. Es el segundo polímero natural más abundante después de la celulosa. Es altamente insoluble en agua y en disolventes orgánicos, debido a los enlaces de hidrógeno que presenta. La quitina se vuelve soluble en ácidos inorgánicos diluidos cuando pierde el acetilo del grupo acetilamino, convirtiéndose en quitosano [1, 2].
El quitosano es un polisacárido catiónico lineal compuesto por unidades de b–(1–4)–2–desoxi–2–amino–D–glucopiranosa (D–glucosamina y b–(1–4)–2–desoxi–2–acetamido–D–glucopiranosa (N–acetil – D– glucosamina). El quitosano se obtiene por deacetilación de la quitina. Las propiedades del quitosano justifican la aplicabilidad de este biopolímero en diversos campos. Los grupos aminos e hidroxilos presentes en su estructura, le confieren la capacidad de derivatización, obteniéndose una variedad de sustancias con propiedades específicas y valiosas en sus respectivos campos de aplicación. Las diversas aplicaciones son: biomédicas, farmacéuticas, en alimentos, en agricultura, en tratamiento de aguas, en cosmética, etc.[3, 4].
En la industria textil se usan muchos colorantes y sus productos de degradación son tóxicos para seres humanos y organismos vivos, la remoción de colorantes de las aguas residuales ha recibido considerable atención en las últimas décadas. Los colorantes sintéticos se degradan por diferentes métodos, como la oxidación, el enzimático, etc., por lo que el tratamiento de aguas residuales aeróbicas no puede eliminar completamente el color de las aguas residuales, o el proceso es muy lento. Uno de ellos es el azul de metileno (AM), colorante de naturaleza catiónica, comúnmente usado en la industria textil para la coloración de algodón, lana, madera, papel y seda. Se considera un compuesto con efectos colaterales adversos a la salud, pues aumenta la frecuencia cardiaca, produce alteraciones gástricas y nerviosas.
MATERIALES Y MÉTODOS
La muestra. Los residuos de cabezas de langostino (Litopanaeus vannamei) proporcionada por la empresa Congelados Pacífico S.A.
Materiales y reactivos. Para la caracterización de la quitina y el quitosano y otros reactivos, hemos utilizados reactivos de grado analítico de la casa Merck.
Equipos. Para la caracterización de la quitina y quitosano se utilizó un espectrómetro infrarrojo, FTIR, Serie 1600, Perkin Elmer; un espectrofotómetro de resonancia magnética nuclear RMN Bruker AC–300 y un espectrofotómetro UV–Visible.
Obtención de la quitina. Para obtener la quitina, a partir de las cabezas de los langostinos, (Litopanaeus vannamei), se realizaron los dos procesos siguientes:
Proceso de desproteinización (DP). Las cabezas así húmedas, fueron tratados con disoluciones de NaOH (4, 8, 12, y 16%); la temperatura de las pruebas fue a temperatura ambiente, para el tiempo se realizaron pruebas de 0,5, 1, 2, y 3 horas. Después de estas pruebas se determinaron las condiciones óptimas. Después de cada proceso, la solución fue filtrada y el material sólido se lavó con agua sucesivamente hasta alcanzar pH neutro. Todas las soluciones básicas se guardan [5].
Proceso de desmineralización (DM). Se lleva a cabo a temperatura ambiente, con HCl a dife-rentes concentraciones (2, 4, 8, y 10%) y el tiempo de reacción se realizaron pruebas de 30, 45, 60, y 75 minutos. Después de cada proceso, la solución se filtra y se lava con agua hasta obtener una solu-ción pH igual que del agua [5].
Obtención del quitosano. El producto obtenido después de realizar la DP y DM se llama quitina, luego se realizó el proceso llamado desacetilación [6] el cual consistió en tratar con soluciones de NaOH (se hizo pruebas con 45, 48, y 50%) el tiempo de reacción se ha variado de 1 hasta 4 horas, la temperatura se mantenido de 95 – 100°C. Después de cada proceso, la solución fue filtrada y el material sólido se lavó con agua sucesivamente hasta alcanzar pH neutro, obteniéndose quitosano de color blanco [6]. La solución básica se ha guardado para otros procesos.
Para obtener el quitosano calcáreo se realizó sólo la desproteinización a las cabezas de langostino y luego la desacetilación, todo ello en las condiciones óptimas previamente determinadas.
Caracterización de la quitina y el quitosano. Para ello se realizaron los siguientes análisis:
- Determinación de Nitrógeno. La determinación del contenido de nitrógeno se realizó por el método de Kjeldahl [7].
- Determinación del porcentaje de humedad. Se determina normalmente por gravimetría; para ello, se lleva a peso constante una muestra calentada en una estufa a 105 ºC, durante 4 horas[7].
- Determinación de cenizas. Esta determinación permite conocer el contenido de materiales inorgánicos presentes en la muestra. Es un parámetro muy importante al momento de evaluar las aplicaciones de un determinado quitosano o quitina. El contenido de cenizas se determina gravimétricamente partir del residuo obtenido tras la combustión de la muestra, durante al menos 6 horas a la temperatura de 800ºC [1, 2].
Determinación del grado de desacetilación. Muchas de las aplicaciones de los quitosanos están estrechamente relacionadas al grado de deacetilación. Existen varios métodos para determinar el grado de deacetilación del quitosano. Algunos de ellos son: espectroscopia UV, espectroscopia IR, RMN y los métodos electroquímicos [1, 8].
Espectroscopia IR. Debido a su simplicidad, es uno de los métodos más empleados. Este método se aplica especialmente cuando se tiene muestras que no se pueden preparar soluciones acuosas acidas, como es el caso de las quitinas, para ello se prepara una mezcla sólida al 2%, 100 mg con KBr. Este método consiste en correlacionar la relación de absorbencias entre dos bandas de absorción determinadas, con el porcentaje de acetilación de la quitina o quitosano. La selección de las bandas de absorción involucra una señal que depende del grado de N–acetilación (normalmente, una de las bandas amida) y otra que sirve de referencia interna para corregir las diferencias de grosor de las películas o de concentración en las pastillas de KBr [7]. Se aplicó esta metodología para la quitina y el quitosano; para ello se tomó como banda característica a la localizada a 1.320 cm–1, y como referencia la banda a 1.420 cm–1, en donde existe una correlación lineal que viene expresada por la siguiente relación [8]:
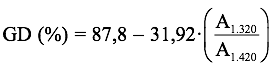
donde GD es el grado de desacetilación, A1320 el área de la banda a 1.320 cm–1 y A1420 el área de la banda a 1.420 cm–1. En todas las determinaciones por IR, es muy importante la selección adecuada de las líneas base en el cálculo de la absorbancia para alcanzar buenos resultados.
Espectroscopia RMN. La espectroscopia de alta resolución es un método no invasivo muy útil para el estudio de las estructuras químicas y estéricas de los polisacáridos. La caracterización por RMN es simple y rápida para análisis de rutina en el laboratorio. En la parte experimental se pesa 2 mg de muestra y se disuelve en una solución ácida (HCl en D2O), luego se pasa por el equipo a 70 °C. El método de determinación del grado de acetilación del quitosano ha sido descrito por Lavertu y col. [9] para el cálculo se usa la fórmula:
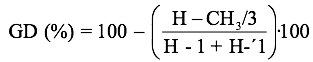
donde GD es el grado de desacetilación, H–CH3 el valor del área bajo la curva de la señal del protón metílico, H–1 el área de la curva del protón con desplazamiento alrededor de 5,2 ppm, y H–’1 el área de la curva del protón con desplazamiento alrededor de 5,4 ppm.
Espectroscopia UV – primera derivada. Este método fue propuesto en 1985 por Muzzarelli y Rochetti y hace uso de la primera derivada de los espectros UV de la N–acetil–D–glucosamina (NAG), del quitosano y de disoluciones de ácido acético. El grado de acetilación se calcula haciendo uso de la ecuación siguiente, que relaciona la concentración de NAG determinada por medio de la curva patrón y la concentración de quitosano empleada en el ensayo [8, 10]:
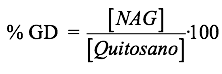
Determinación del peso molecular. El método viscosimétrico es uno de los más empleados en las determinaciones de pesos moleculares de polímeros, por su exactitud y sencillez, y puede ser aplicado a todo el intervalo de masas macromoleculares, exceptuando el caso de macromoléculas esféricas o muy ramificadas, ya que en ellas la viscosidad es independiente del peso molecular. Primero se determina las viscosidades empleando la formula: η = K·ρ·t, donde η es la viscosidad, K es una constante, ρ es la densidad y t el tiempo de caída en segundos. A continuación, se calcula la viscosidad intrínseca, para finalmente determinar el tamaño molecular de los polímeros, que se relaciona con el peso molecular mediante la ecuación de Mark–Houwink–Sakurada [11].
El análisis de la absorción del azul de metileno, se preparó una solución de 200 ppm. Los absorbentes (quitosano Ch y quitosano calcáreo ChCa), previamente caracterizados se procedió a molerlo, luego se tamizó a una malla de 10–20 mesh. En la etapa de las pruebas de absorción, se realizó teniendo como variables a los siguientes parámetros (manteniendo constante 100 mL de la solución de metileno a 200 ppm): tiempo de agitación, velocidad de agitación, cantidad de adsorbente, etc.
RESULTADOS Y DISCUSIONES
Caracterización de la muestra (cabezas del langostino Litopanaeus vannamei) fue determinando sus porcentajes de humedad, cenizas, nitrógeno, quitina, quitosano, y quitosano calcáreo obtenido; estos resultados se muestran en la Tabla 1. Además, en esta tabla se observan los porcentajes de quitina, quitosano, y quitosano calcáreo obtenidos, esto significa los rendimientos de quitina y quitosano, ver Tabla 1.
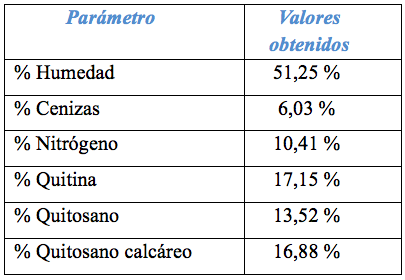
Los procesos de obtención de quitina, quitosano y quitosano calcáreo se realizaron en un reactor, el cual es un tanque cilíndrico de acero inoxidable de 75 L de capacidad que cuenta con un sistema electrónico de control de temperatura, paletas de agitación y selector de velocidad. La muestra, cabezas de langostino, se trabajó tal como la empresa langostinera lo desecha, donde su humedad es alta, alrededor de 52%, además contiene carotenos, proteínas, grasas, etc.
Para el proceso de desproteinización, se procedió a tratar la muestra con hidróxido de sodio y este proceso genera calor, así la temperatura llega a un máximo de 48°C; también durante el proceso se puede ir sacando muestras para ver cualitativamente si ya desproteinizó totalmente o no, además, se analizó la alícuota de 20 mL (previamente filtrada), para determinar el porcentaje de proteína usando el reactivo de Biuret y aplicando la espectroscopia ultravioleta visible. Al final, se obtuvo que la desproteinización optima es con NaOH al 10% p/p, 90 minutos de agitación a 180 rpm.
En el proceso de desmineralización con el HCl, se debe tener en cuenta la liberación de dióxido de carbono a partir de la reacción ácida del carbonato de calcio o magnesio contenido en las cabezas de langostino. Para obtener los parámetros óptimos de este proceso, se tuvo que extraer una alícuota periódicamente y analizar el porcentaje de sólidos, la variación del pH y así hacer una curva y encontrar el parámetro óptimo. Por ejemplo, cuando se trabaja con HCl al 6% v/v, para obtener el tiempo optimo se tomó alícuotas de 20 mL de solución de la mezcla reaccional periódicamente se filtró con papel de filtro rápido y se eliminó el agua colocándole en una estufa a 40 °C, durante 2 días, esto se realizó por triplicado, luego se determinó el peso en promedio y observando la gráfica (ver Figura 1 y Tabla 2) se determinó el tiempo óptimo que es de 30 minutos [8].
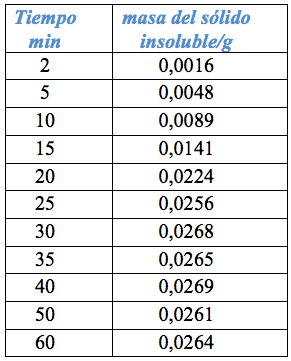
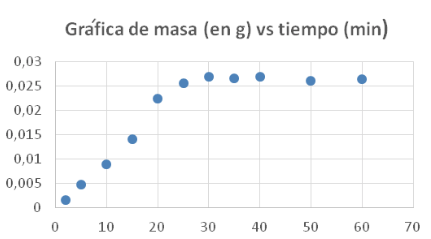
Con este mismo sistema trabajó para los otros parámetros. Finalmente, las condiciones óptimas del proceso de desmineralización son: 30 minutos, HCl al 6% v/v, 150 rpm y a temperatura ambiente.
En el proceso de desacetilación para obtener el quitosano también se trabajó de la misma manera que los dos procesos anteriores, se tomó periódicamente alícuotas de 25 mL de solución de NaOH de la mezcla reaccionante (previamente filtrada), luego esta alícuota se diluye a 500 mL, luego se toma una alícuota de 50 mL, el cual se tituló con HCl 0,25 M, previamente valorado. Después estos valores (ver Tabla 3), tiempo de reacción y volumen de HCl gastado, se grafican, tal como se observa en la Figura 2 y Tabla 3.
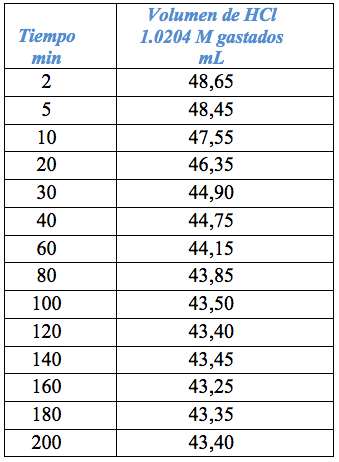
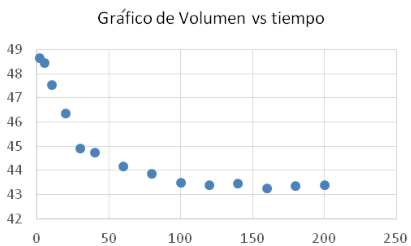
Todos los procesos de obtención la quitina y el quitosano son ecológicos y ecoeficientes ya que no generan residuos, los residuos (soluciones acuosas acidas y básicas, tanto de los filtrados como de los lavados) siempre se guardan ya sea para reutilizarlos (como los residuos de desacetilación); o se reúnen para formar otro subproductos (como los residuos de la desmineralización y desproteinización), en este caso se lleva al punto isoeléctrico; el subproducto formado se puede usar en alimentos balanceados para aves, ya que contiene principalmente proteínas, sales de calcio y carotenos (astaxantina).
La caracterización de los biopolímeros (quitina, quitosano y quitosano calcáreo) se realizó determinando su porcentaje de humedad, cenizas, nitrógeno, desacetilación, viscosidad, masa molecular según las referencias; todos estos resultados en forma resumida están en la Tabla 4.
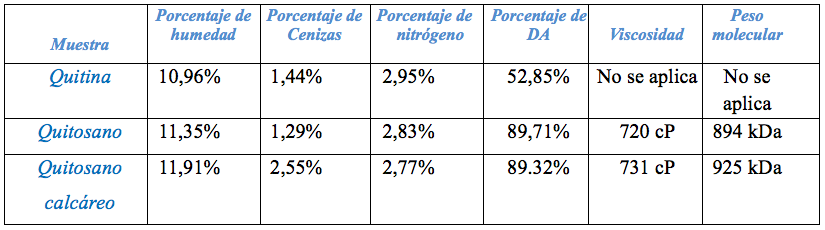
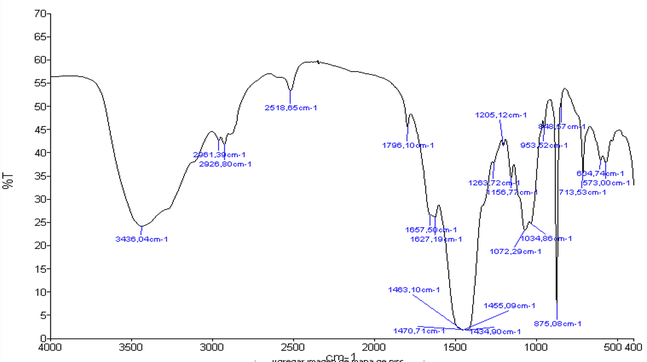
Para el caso de la determinación del porcentaje de DA hay tres métodos: En el caso de la espectroscopia IR, las muestras se molieron y tamizaron hasta tener un tamaño de malla 100, luego, se añadió KBr en una relación de 2:98 p/p, la mezcla fue prensada hasta obtener una pastilla muy delgada y traslúcida, que fue usada para obtener el espectro de la quitina, analizando sus bandas se identifican las bandas características: banda del O–H a 3.434, N–H alrededor de 3.200, C–H a 2.920 banda de la amida I a 1.657 y 1.627 cm–1 , banda N–H a 1.434, C–O–C a 1.072 y a 848 cm–1 bandas de la tensión de los grupos anoméricos (ver Figura 3a). Luego, aplicamos las fórmulas para calcular el grado de desacetilación, así tenemos para 52,85% para la quitina. Para los otros biopolímeros se realizan los otros dos métodos [12].
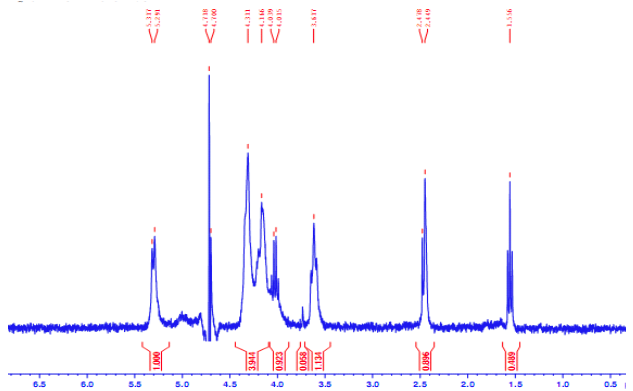
La metodología para determinar el porcentaje de DA por RMN–H presenta las siguientes ventajas: buena en precisión, especificidad, estabilidad y exactitud; por ello esta técnica 1H–RMN hace que los valores obtenidos para el grado de acetilación sean los tomados en cuenta para la determinación de los pesos moleculares por viscosimetría. En el método 1H–RMN, no necesita conocerse la cantidad de muestra, puesto que esto no interfiere con las señales relevantes del quitosano. Las señales usadas para la determinación del grado de acetilación están bien resueltas, y, por tanto, esta técnica es precisa y exacta, aún cuando se usen diferentes combinaciones de señales. En la Figura 3b, se muestra el espectro del quitosano calcáreo, se aplicaron las formulas respectivas para calcular el grado de desacetilación, obteniéndose el porcentaje de DA de 89,32% y para el quitosano de 89,71%.
Además, se aplicó la espectroscopia UV – primera derivada para obtener el porcentaje de DA. En esta técnica, se debe tener en cuenta que los resultados dependen de la exactitud en el peso de la muestra. Para conocer el %DA de la muestra se prepararon disoluciones de ácido acético 0,01 M, 0,02 M y 0,03 M y disoluciones patrón de N–acetil–glucosamina (NAG) de 10, 20, 30 y 40 ppm en ácido acético 0,01 M. Se registraron los espectros UV – primera derivada de estas soluciones, según indican las referencias y a partir de estos datos se construyó la curva de calibración [8, 11].
La longitud de onda donde se cruzan las curvas de ácido acético es aproximadamente la misma donde la absorbancia de la NAG es máxima (202,12 nm) y la interferencia del ácido acético es mínima. Con la recta de calibración, Figura 10, obtenida al representar las concentraciones de NAG frente a la diferencia de alturas se determinó el porcentaje de DA del quitosano usando la ecuación. Para nuestro caso el porcentaje de DA fue de 89,18% y para el quitosano dio 89,62%.
Para determinar la viscosidad intrínseca se aplicó el método viscosimétrico capilar, y se uso el viscosímetro de Ostwald. Para ello, se preparó una solución de 1 mg/mL de quitosano en una solución 0,1 M de ácido acético y 0,2 M de NaCl, y así se continuó el procedimiento que indica la referencia [8]. Finalmente, se pudo calcular la viscosidad para el quitosano y quitosano calcáreo: 894 KDa y 925 KDa, respectivamente.
El porcentaje de remoción del colorante (%R) se calcula con la ecuación:
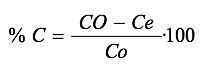
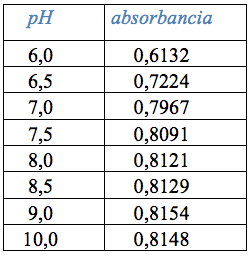
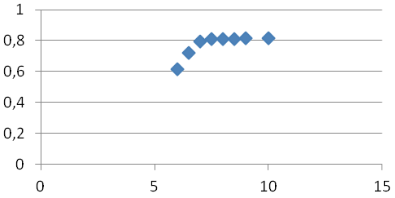
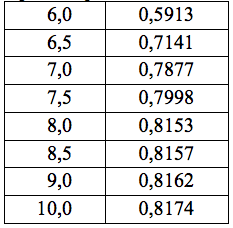
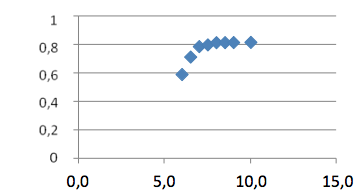
La adsorción se realizó en las siguientes condiciones para el quitosano Ch1020: se colocó 100 mL de disolución de colorante azul de metileno de concentración de 200 ppm, en un vaso de 250 mL, se trabajó por triplicado, luego, se añadieron 200 mg de quitosano, se agitó a 100 rpm, durante un período de 1 hora, pero se varía el pH desde 2 hasta 10 (ver Tabla 5 y Figura 4). De la gráfica se observa que el pH óptimo para adsorción es 7,5. A las mismas condiciones de trabajo para el quitosano calcáreo, estos resultados se observan en la Tabla 6 y Figura 5; de las cuáles se infiere que el pH óptimo de adsorción es de 8,0.
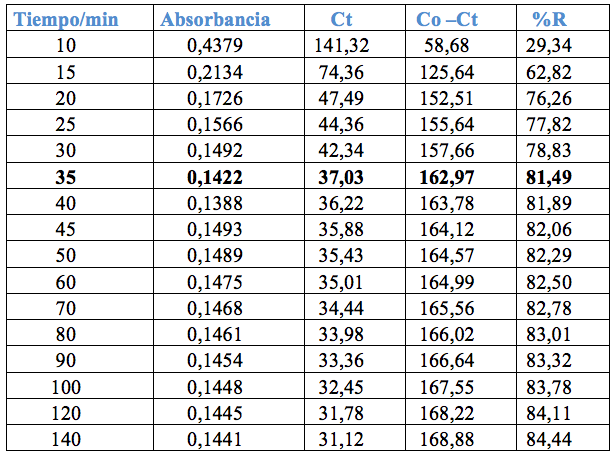
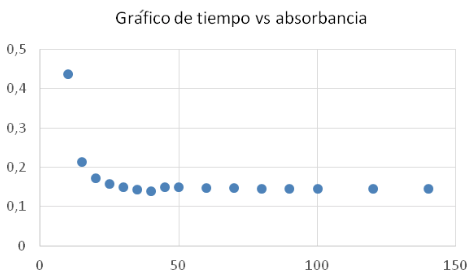
Con los datos encontrados de pH óptimo, se analizó el tiempo óptimo, para ello, se realizó la adsorción a las siguientes condiciones: se colocó 100 mL de solución de colorante azul de metileno de concentración de 200 ppm, en un vaso de 250 mL, se trabajó por triplicado, luego se añadió 200 mg de quitosano, se agita a 100 rpm, durante un período de 3 horas, pero se realizó el muestreo de una alícuota cada 30 minutos a pH 7,5 para el quitosano y pH 8,0 para el quitosano calcáreo, respectivamente. Los resultados se muestran en la Figura 6 y Tabla 7. De estos datos se observa que a los 30 minutos se obtuvo una adsorción del 77% aproximadamente y luego hay un ligero aumento de adsorción.
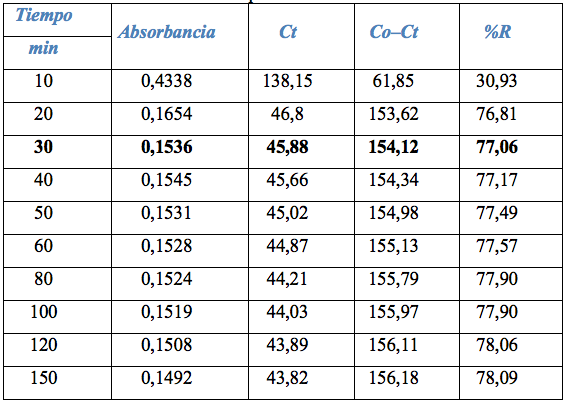
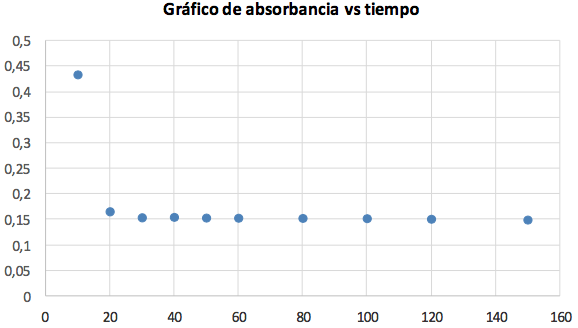
Finalmente, se obtuvieron porcentajes significativos de adsorción del colorante (azul de metileno de 200 ppm), así, para el quitosano Ch1020, se observa que, a los 30 minutos, fue adsorbido el 77% a un pH óptimo de 7,5; mientras que para el quitosano calcáreo ChCa 1020 se observa un máximo de adsorción del 81% a los 35 minutos, a pH 8,0.
CONCLUSIONES
Se han obtenido biopolímeros a partir de cabezas de langostino a nivel piloto, se obtuvo quitosano calcáreo con 89% de DA, peso molecular de 925 kDa y quitosano con el mismo porcentaje de DA pero con peso molecular ligeramente menor (894 kDa).
Se obtuvieron porcentajes significativos de adsorción del colorante (azul de metileno de 200 ppm), así, para el quitosano Ch1020 se observa, que a los 30 minutos, fue adsorbido el 77% a un pH óptimo de 7,5; mientras que para el quitosano calcáreo ChCa 1020 se observa un máximo de adsorción del 81% a los 35 minutos a pH 8,0.
BIBLIOGRAFÍA
[1] Pastor A “Quitina y quitosano: obtención, caracterización y aplicaciones”. CYTED, Lima, Fondo Editorial de la Pontificia Universidad Católica del Perú, 2004
[2] Kumar M, Muzzarelli R, Muzarelli C, Sashiwa H, Domb A, Chem Rev., 104, 6017 (2004)
[3] Percot A, Viton C Y Domard A, Biomacromolecules, 4,1380 (2003)
[4] Chang K, Carbohydrate Research, 303, 327 (1997)
[5] AOAC, Official methods of analysis of the Association of Official Analytical Chemists, 15th ed., 1990
[6] A.S.T.M “Standard Test Method for Total Nitrogen in Organic Materials by Modified Kjeldahl Met-hod”, A.S.T.M Designation E 258 – 67 (Reapproved 1987)
[7] Brugnerotto J, Lizardi J, Goycoolea F, Argüelles W, Desbrieres J, Rinaudo M, Polymer, 42, 3569 (2001)
[8] Castro O “Investigacion aplicada con quitina y quitosano”. Editorial Académica Española, España, 2017
[9] Lavertu M, Xia A, Serreqi A, Berrada M, Rodrigues A, Wang D, Bushman M, Gupta AA, J Pharm Biom Research, 32, 1149 (2003)
[10] Muzzarelli R, Rochetti R, Carbohydrate Polymer, 5, 461 (1985)
[11] Fernandez E, Novoa R, Quiñoa E, Riguera R, Carbohydrate Polymers, 61, 155 (2007)
[12] Roberts G, Domszy J, Int J. Biol Macromol., 4, 374 (1982)
